
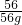 =
=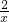
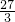 ×2=18,钠的二价相对原子质量为
×2=18,钠的二价相对原子质量为 ×2=46,相对原子质量越大,产生的氢气质量越小,BCD的二价相对原子质量均比铁的小,故产生的氢气比铁多,故B、C、D错误,所以本题应选A.
×2=46,相对原子质量越大,产生的氢气质量越小,BCD的二价相对原子质量均比铁的小,故产生的氢气比铁多,故B、C、D错误,所以本题应选A.

科目:初中化学 来源:专题突破训练_初三化学强化系列03(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com