


科目:初中化学 来源: 题型:
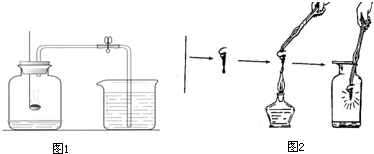 (1)如图1,用红磷燃烧来测定空气中氧气的含量,实验过程中发生的实验现象是:
(1)如图1,用红磷燃烧来测定空气中氧气的含量,实验过程中发生的实验现象是:| 点燃 |
| 点燃 |
| 点燃 |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
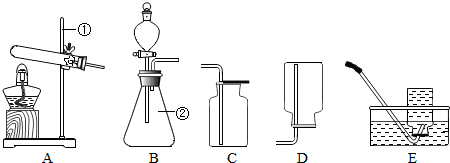
| ||
| ||
| 编号 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取反应后固体剩余物0.2g加入5mL 6%的H2O2溶液中 | 剧烈反应,放出大量热量,产生大量气体 | 生成物中的MnO2催化分解H2O2 |
| 2 | 取0.2gMnO2加入5mL a a (H2O2质量分数)的H2O2溶液中 |
平稳反应,发出热量,持续产生气体 | MnO2催化分解H2O2 |
| 3 | 取反应后固体剩余物1.0g加入足量水中,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | b b |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:化学教研室 题型:038

|
稀盐酸的用量 |
剩余固体的质量 |
|
第一次加入5mL |
1.5g |
|
第二次加入5mL |
1.0g |
|
第三次加入5mL |
0.5g |
|
第四次加入5mL |
0.3g |
|
第五次加入5mL |
0.3g |
计算:(1)该石灰石样品中碳酸钙的质量分数。
(2)如果该石灰厂煅烧60t这种石灰石,最多可得到含杂质的生石灰多少吨?同时能得到副产品二氧化碳多少吨?
查看答案和解析>>
科目:初中化学 来源:2012-2013学年湖北省襄阳市宜城市流水中学九年级(上)第一次月考化学试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com