
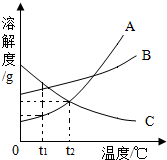
 如图A、B、C为三种物质的溶解度曲线,据图回答:
如图A、B、C为三种物质的溶解度曲线,据图回答:分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
饱和溶液和不饱和溶液之间可以相互转化;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否析出固体;
从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶;
根据物质的溶解度曲线可以判断随着温度的变化,溶质质量分数变化的情况.
解答 解:(1)t1℃时,A、B、C三种物质的溶解度由小到大顺序是A、B、C;
t1℃时,将4.2gA物质溶于20g水中,刚好形成饱和溶液,则t1℃时,A物质的溶解度为:4.2g×5=21g;
在不改变C溶液质量的条件下,将C的饱和溶液转化处不饱和溶液的方法是降低温度.
故填:A、B、C;21;降低温度.
(2)将t2℃时的等质量三种物质的饱和溶液分别降到0℃时,A物质的溶解度差最大,因此析出溶质最多,C的溶解度随着温度的降低而增大,因此无溶质析出.
故填:A;C.
(3)由溶解度曲线可知,A的溶解度受温度变化影响较大,B的溶解度受温度变化影响较小,当A中含有少量B时,为了得到纯净的A,可采用降温结晶的方法.
故填:降温结晶.
(4)t1℃时,B的溶解度大于A的溶解度,并且仍然都是饱和溶液,因此B的质量分数大于A的质量分数;
C在t2℃时的溶解度大于A在t1℃时的溶解度,小于B在t1℃时的溶解度,因此t1℃时,C的质量分数小于B,大于A,所以若将t2℃三种物质的饱和溶液分别降到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是B、C、A.
故填:B、C、A.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
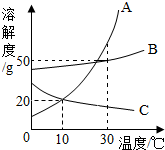 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 30℃时,A、B、C三种物质的溶解度曲线由大到小的顺序是:A>B>C | |
| B. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| C. | 10℃时,A、B、C三种饱和溶液同时升温到30℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| D. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,析出的晶体质量大到小的顺序一定是:A>B>C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 为测定某黄铜(铜锌合金)中锌的质量分数,某校研究小组取10g样品置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中物质的总质量与加入稀硫酸的质量关系如图所示.请计算:
为测定某黄铜(铜锌合金)中锌的质量分数,某校研究小组取10g样品置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中物质的总质量与加入稀硫酸的质量关系如图所示.请计算:查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单宁酸由碳、氢、氧三种元素组成,属于有机物 | |
| B. | 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 | |
| C. | 单宁酸中碳元素的质量分数是53.6% | |
| D. | 一个单宁酸分子中含26个氢分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com