暗紫色固体A在加热的条件下反应生成B和C以及D,常温下过氧化氢溶液遇到C时分解放出D,其中C在反应前后的质量和化学性质都没有改变,若将细铁丝放在D中点燃能剧烈燃烧,火星四射,生成黑色固体E.
(1)写出下列物质的化学式:A ;E .
(2)用文字表达式表示有关的化学反应,并指出反应所属的类型(化合反应、分解反应):
① ( 反应);
② ( 反应);
③ ( 反应).
(3)C是过氧化氢反应中的 .(填“催化剂”或“氧化剂”)
【答案】
分析:在反应前后质量和化学性质没有改变,说明C在反应中起催化作用;暗紫色固体A是高锰酸钾,E是四氧化三铁,从而可以判断出A是高锰酸钾,B是锰酸钾,C是二氧化锰,D是氧气,E是四氧化三铁,据此回答下面的问题.
解答:解:
(1)氯酸钾在二氧化锰做催化剂的情况下加热能生成氯化钾和氧气,所以A、B、C、D、E、F分别是高锰酸钾、锰酸钾、二氧化锰、氧气、四氧化三铁.故填:高锰酸钾;四氧化三铁.
(2)①高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气.
故答案为:2KMnO
4 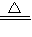
K
2MnO
4 +MnO
2 +O
2↑;
②实验室用过氧化氢溶液制氧气生成水和氧气.故答案为:2H
2O
2 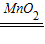
2H
2O+O
2↑;
③细铁丝在氧气中燃烧生成四氧化三铁,故答案为:3Fe+2O
2 
Fe
3O
4.
(3)常温下过氧化氢溶液遇到C时分解放出氧气,其中C在反应前后的质量和化学性质都没有改变,故C是二氧化锰,该反应的催化剂.
点评:解答本题要掌握各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.

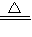 K2MnO4 +MnO2 +O2↑;
K2MnO4 +MnO2 +O2↑;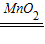 2H2O+O2↑;
2H2O+O2↑; Fe3O4.
Fe3O4.

 阅读快车系列答案
阅读快车系列答案