
分析 加入稀盐酸时,石灰石样品中的碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳;根据质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳质量,据此根据反应的化学方程式列式计算出参加反应的碳酸钙的质量,进而计算出石灰石样品中碳酸钙的质量分数.
解答 解:(1)生成CO2的质量为10g+50g-56.7g=3.3g.故答案为:3.3g.
(2)设石灰石样品中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{x}=\frac{44}{3.3g}$
x=7.5g
石灰石样品中碳酸钙的质量分数为:$\frac{7.5g}{10g}$×100%=75%.
答:石灰石样品中碳酸钙的质量分数为75%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:选择题
| A. | 氧气具有可燃性,可用于炼钢、航天 | |
| B. | 氮气的化学性质稳定,常用作保护气 | |
| C. | 铜导电性良好,可用于制导线 | |
| D. | 氖气通电时能发出带颜色光,可用于霓虹灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某同学学习了二氧化碳的知识后,对二氧化碳的性质进行如下探究.
某同学学习了二氧化碳的知识后,对二氧化碳的性质进行如下探究.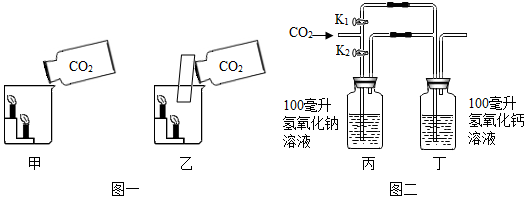
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com