
CO和CH4的混合气体共44g,充分燃烧后冷却至室温,得到88g气体,求原混合气体中CO和CH4各多少克?
|
解答:CO质量为28g,CH4质量为16g. |
|
点悟:点燃生成CO2和H2O,冷却至室温,水蒸气液化,88g气体为CO2.若利用化学方程式计算则需设CO质量为x,它生成CO2,质量为y. 2CO+O2 2×28 2×44 x y 2×28y=2×44x ① CH4+2CO2 16 44 44g-x 88g-y 16(88g-y)=44(44g-x) ② 解:①、②得出x=28g,44g-x=16g,较麻烦 若利用质量守恒关系,生成的88g CO2中的C元素分别来自于质量为x的CO及质量为(44g-x)的CH4,则: 88g× 88g× 解得x=28g 44g-x=16g |


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:阅读理解

| 装置D的质量 | 装置E的质量 | |
| 反应前 | 292.4g | 198.2g |
| 反应后 | 296.0g | 201.5g |

查看答案和解析>>
科目:初中化学 来源: 题型:
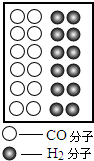 (2011?茂名)煤、石油、天然气是我国最主要的化石燃料,它们都是不可再生能源,故如何高效使用化石燃料以及开发新能源是我国当前重要的研究课题.
(2011?茂名)煤、石油、天然气是我国最主要的化石燃料,它们都是不可再生能源,故如何高效使用化石燃料以及开发新能源是我国当前重要的研究课题.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程.
(2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程.
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
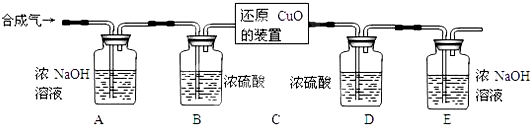
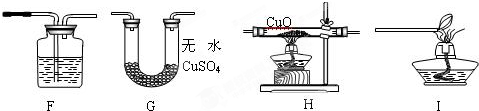
| 装置D的质量 | 装置E的质量 | |
| 反应前 | 292.4g | 198.2g |
| 反应后 | 296.0g | 201.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:
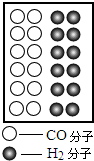 煤、石油、天然气是我国最主要的化石燃料,是不可再生产的能源,故如何高效利用化石燃料以及开发能源是我们当前重要的研究课题
煤、石油、天然气是我国最主要的化石燃料,是不可再生产的能源,故如何高效利用化石燃料以及开发能源是我们当前重要的研究课题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com