
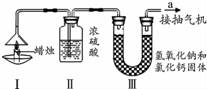
 为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如下图所示的实验.实验步骤如下:先分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量.按图示连接好仪器装置,点燃蜡烛,同时从a导管抽气.一段时间后熄灭蜡烛,再分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量.(提示:浓硫酸只吸收水,氢氧化钠和氯化钙固体即可以吸收水分也可以吸收二氧化碳)实验数据如表.
为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如下图所示的实验.实验步骤如下:先分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量.按图示连接好仪器装置,点燃蜡烛,同时从a导管抽气.一段时间后熄灭蜡烛,再分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量.(提示:浓硫酸只吸收水,氢氧化钠和氯化钙固体即可以吸收水分也可以吸收二氧化碳)实验数据如表.| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216. |
分析 (1)浓硫酸有很强的吸水性;氢氧化钠和氧化钙固体可吸收二氧化碳气体;根据表格中反应后的质量减去反应前的物质质量,即可得出反应后生成的水和二氧化碳的质量;
(2)根据水和二氧化碳的质量可以求出石蜡中碳元素的质量以及氢元素的质量进行解答;
(3)考虑蜡烛的燃烧需要氧气,根据质量守恒定律去解释;
(4)根据空气中也含有水蒸气和二氧化碳进行解答.
解答 解:(1)浓硫酸有很强的吸水性.可以吸收蜡烛燃烧后产生的水蒸气;氢氧化钠和氧化钙固体可吸收蜡烛燃烧后生成的二氧化碳气体.所以装置I和II增加的质量分别是水和二氧化碳的质量,反应后生成的水:184.1-182.3=1.8g;反应后生成的二氧化碳:216.6-212.2=4.4g.故答案为:1.8;4.4;
(2)碳元素的质量为:4.4g×$\frac{12}{44}$×100%=1.2g.氢元素的质量为:1.8g×$\frac{2}{18}$×100%=0.2g
蜡烛中碳元素和氢元素的质量比为:1.2g:0.2g=6:1;故填:6:1;
(3)蜡烛的燃烧需要氧气,氧气来自空气中,根据质量守恒定律,参加反应的各物质的质量和等于生成的各物质的质量和,消耗的蜡烛+氧气=水+二氧化碳,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛减少的质量,是因为有了氧气的参加.
故答案为:蜡烛燃烧时,氧气也参与反应,故理论上,装置II和III增加的质量等于消耗的蜡烛和氧气的总质量;
(4)该实验不能准确测出蜡烛燃烧生成二氧化碳和水的质量,原因是空气中水蒸气和二氧化碳也分别被吸收到装置Ⅱ和装置Ⅲ中.故填:不能;空气中水蒸气和二氧化碳也分别被吸收到装置Ⅱ和装置Ⅲ中.
点评 本题以实验探究的形式考查蜡烛燃烧后生成物中碳、氢两种元素的质量比.题目虽不算太难,但仍需同学们细心考虑.


科目:初中化学 来源: 题型:选择题
| A. | 若M为单质,N为化合物,则该反应一定是置换反应 | |
| B. | 数值x与y的和等于m与n的和 | |
| C. | 若该反应是复分解反应,则M、N、P、Q一定是化合物 | |
| D. | 若反应物M失氧,则该反应可能是化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
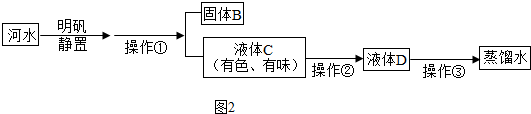
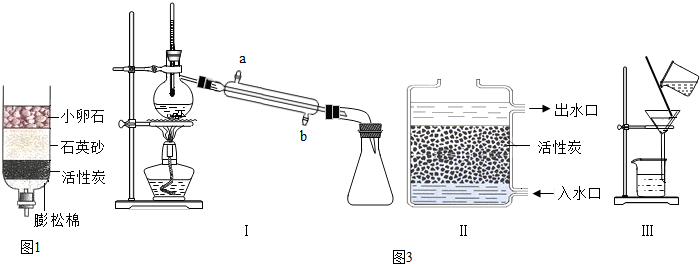
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
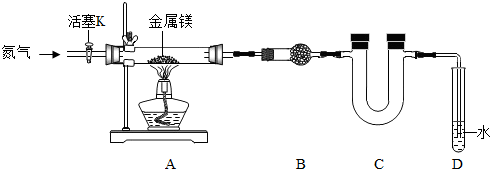
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
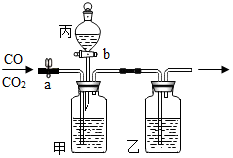 在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白.
在实验室用如图所示装置进行CO和CO2的分离和干燥.现只有稀盐酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
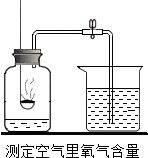 法国化学家拉瓦锡通过实验得出的结论是氧气约占空气总体积的$\frac{1}{5}$.某同学用如图装置进行验证,实验后发现气体减少的体积小于$\frac{1}{5}$,请你帮助这位同学找出两种可能造成这样结果的原因:
法国化学家拉瓦锡通过实验得出的结论是氧气约占空气总体积的$\frac{1}{5}$.某同学用如图装置进行验证,实验后发现气体减少的体积小于$\frac{1}{5}$,请你帮助这位同学找出两种可能造成这样结果的原因:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | N2O | B. | NO2 | C. | N2O | D. | N2O5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com