

| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g•L-1 | 脱硫率/% |
| Ⅰ | 23 | 2.5% | 99.5 |
| Ⅱ | 23 | 3.2% | 97.1 |
| Ⅲ | 40 | 2.5% | 94.3 |
分析 (1)二氧化硫排放到空气中,容易产生的环境问题是形成酸雨;
(2)根据在化合物中正负化合价代数和为零,结合亚硫酸的化学式进行解答本题;
(3)熟石灰中和稀硫酸生成硫酸钙和水,据此写成方程式;
(4)脱硫率与温度、含硫烟气SO2浓度的关系,应在相同温度比较不同浓度的影响,以及相同浓度不同温度的影响.
解答 解:(1)二氧化硫排放到空气中,容易产生的环境问题是形成酸雨;故选A;
(2)氧元素显-2价,氢元素为+1价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:1×2+x+(-2)×3=0,则x=+4价;
(3)熟石灰中和稀硫酸生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O;
(4)由表中数据可知得出的结论是:浓度一定时,温度升高,脱硫率降低;温度一定时,烟气中SO2浓度升高,脱硫率降低.
故答案为:(1)A;
(2)+4;
(3)Ca(OH)2+H2SO4═CaSO4+2H2O;
(4)浓度一定时,温度升高,脱硫率降低;温度一定时,烟气中SO2浓度升高,脱硫率降低.
点评 本题考查的知识点较多,要认真分析工艺流程图,明确其中反应的过程,本题有一定的难度.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
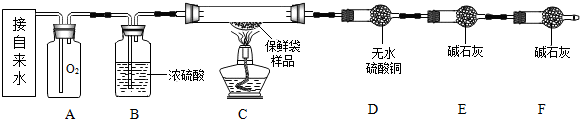
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
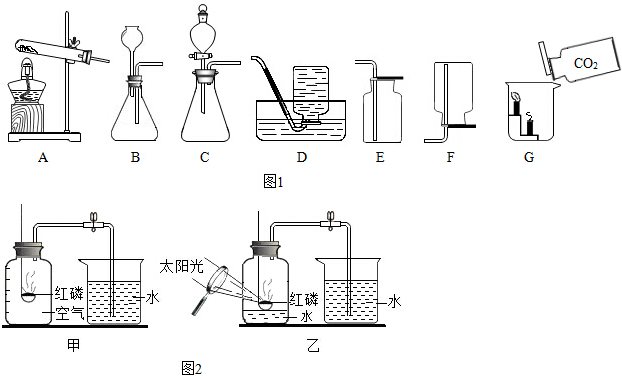
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
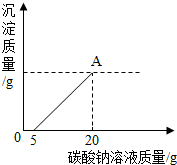 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  木质桌椅 | B. |  大理石雕塑 | C. |  黄金首饰 | D. |  塑料盆 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
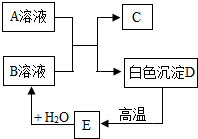 竹海丰富的林竹资源为四川永丰纸业股份有限公司提供了充足的原材料,而造纸工业中常常用到氢氧化钠和碳酸钠等原料.
竹海丰富的林竹资源为四川永丰纸业股份有限公司提供了充足的原材料,而造纸工业中常常用到氢氧化钠和碳酸钠等原料.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下一氧化碳能还原氧化铁生成铁 | Ⅰ对;Ⅱ对 |
| C | 铁比铝更易锈蚀 | 铝比铁活泼 | Ⅰ错;Ⅱ对 |
| D | 铝在空气中表面生成致密氧化膜 | 不能用铝罐储存运输稀硫酸、稀盐酸 | Ⅰ错;Ⅱ对 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com