
【题目】加热一定量高锰酸钾制氧气,下图所示的有关数量关系,与反应事实不相符的是
A.  B.
B.  C.
C. 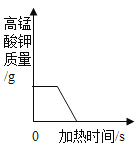 D.
D. 
【答案】B
【解析】
根据加热一定量的高锰酸钾制取氧气的化学方程式:![]() 可知:氧气的质量逐渐增加,当高锰酸钾反应完,则不变;剩余固体的质量逐渐减小,当高锰酸钾分解完毕则不变;锰元素存在于固体中,其质量不变;剩余固体中氧元素的含量逐渐减小直到反应完,则不变。
可知:氧气的质量逐渐增加,当高锰酸钾反应完,则不变;剩余固体的质量逐渐减小,当高锰酸钾分解完毕则不变;锰元素存在于固体中,其质量不变;剩余固体中氧元素的含量逐渐减小直到反应完,则不变。
A、随着反应的进行,氧气的质量逐渐增加,当高锰酸钾反应完,则不再增加,氧气质量不会一直增加,故A正确;
B、高锰酸钾分解,有部分氧元素转化为氧气逸出,所以剩余固体中氧元素的含量逐渐减小,待反应完,则不变,氧元素的含量不会为零,故B错误;
C、高锰酸钾分解,有氧气逸出,质量逐渐减小,当高锰酸钾反应完,质量为0,故C正确;
D、剩余固体的质量逐渐减小,当高锰酸钾分解完毕,则不再减小,剩余固体不会是0,故D正确。
故选:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】利用空气制取氨肥的流程如图所示。

(1)利用空气制取氨气和氧气是在低温下加压把空气转变成________态,然后蒸发,________先蒸发出来,该过程属于________变化。(填“物理”或“化学”)
(2)Ⅰ中参加反应的单质甲为________。(填化学式)
(3)写出Ⅱ反应的化学方程式为________________________________________________。
(4)上述Ⅰ.Ⅱ、Ⅲ反应过程中属于化合反应的是________________(填“Ⅰ”“Ⅱ”“Ⅲ”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用如图所示装置制取氧气并完成相关实验(夹持仪器已略去)。
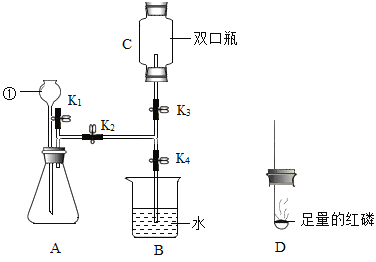
(1)仪器①的名称是_____。
(2) A装置中反应的化学符号表达式为_____
(3)用C装置收集气体的方法是_____(填序号)。
a.排水法 b.向下排空气法 c.向上排空气法
(4)C中收集满氧气后,打开弹簧夹K1,关闭K2、K3,其中打开K1的目的是_____,点燃 D中燃烧匙内的红磷后立即伸入C装置中并把塞子塞紧,观察到红磷燃烧的现象是_____,待红磷熄灭、C装置冷却后,打开K3、K4,观察到的现象是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】气体的的制备是科学实验基本技能之一。实验室制取二氧化碳所需药品是________和________,反应的文字表达式为______________。
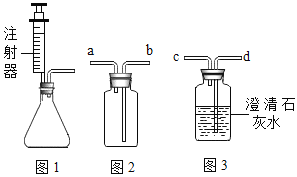
(1)若图1装置制取二氧化碳,其优点是______________。
(2)若图2装置收集二氧化碳,应将气体发生装置的导管与图2装置的导管_______(选填“a”或“b”)相连接。检验该装置中二氧化碳已收集满的操作是_______________。
(3)若用图3装置检验二氧化碳,应将气体发生装置的导管与图3装置的导管_________ (选填“c”或“d”)相连接。写出用澄清石灰水检验二氧化碳的文字表达式_______。
(4)下列二氧化碳的制备装置中,不能起到“能控制反应发生和停止”效果的是________。
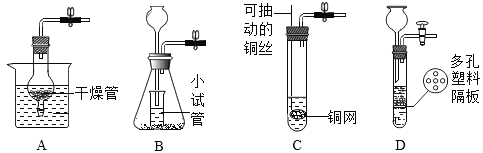
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有实验室制取气体的部分装置,请结合所学化学知识,回答有关问题:
(1)请写图中标有字母的仪器名称:a_______,b _______,c ______;
(2)实验室用高锰酸钾制取氧气,装置A还需做的一点改动是 _____________,请写出该反应的文字表达式:__________________,反应的基本类型属于 ________反应。
(3)实验室用过氧化氢溶液制取氧气,可用的发生装置是 _____,请写出反应的文字表达式:_______________,其中二氧化锰 _____作用.
(4)收集氧气可以选择装置______,原因是___________________.若用D或C装置收集氧气,检验其是否收集满的方法是____________________。
(5)某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作会引起的后果是______________________。
(6)实验室用高锰酸钾制取氧气并用排水法收集氧气,实验结束后,收集到的氧气不纯其原因是:_________________;
(7)实验室常用大理石(固体)与稀盐酸(液体)在常温下制取二氧化碳气体,二氧化碳气体的密度比空气大,且能溶于水,可选用_____装置制备二氧化碳,收集二氧化碳气体时选用装置________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究性学习小组选择“过氧化氢生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
(假设)过氧化氢生成氧气的快慢与催化剂种类有关
(实验方案)常温下,在两瓶体积相同、浓度相同的过氧化氢溶液中分别加入相同质量的二氧化锰和红砖粉,测量各生成一瓶(相同体积)氧气所需要的时间。
(进行实验)图示是他们进行实验的装置图,气体发生装置中A仪器的名称是:_________,此实验中B处宜采用的气体收集方法是_____________。

(实验记录)
实验编号 | 1 | 2 |
反应物 | 6% 过氧化氢 | 6% 过氧化氢 |
催化剂 | 1 g红砖粉 | 1 g 二氧化锰 |
时间 | 152 s | 35 s |
(结论)该探究过程得出的结论_____________________。
(反思)过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快。若要证明二氧化锰和红砖粉是否是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的___________和_________是否变。
过氧化氢生成氧气的快慢还与哪些因素有关?请你帮助他们继续探究。____________ (只要求提出假设和实验方案)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学式造福人类的科学,在生产生活中做出了重大贡献。
(1)一氧化二氮是人类最早应用的麻醉剂之一,描述一氧化二氮化学性质的是_____(填序号)。
A 无色有甜味的气体
B 高温下能分解生成氮气和氧气
C 熔点-90.9℃,沸点-88.5℃
(2)碳酸氢钠(NaHC![]() )是某些抗酸药的有效成分,能够中和人体内多余的胃酸,在碳酸氢钠中有_____种元素。
)是某些抗酸药的有效成分,能够中和人体内多余的胃酸,在碳酸氢钠中有_____种元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用如图所示的装置测定空气中氧气的含量(体积分数)。他的操作过程如下(l00mL和500mL量筒供选用):
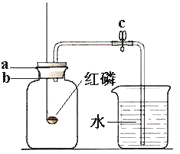
①检查整个装置的气密性后,将c处的止水夹夹紧,点燃红磷后,迅速插入左边的广口瓶中。
②待燃烧停止,整个装置冷却至室温后,将c处的止水夹打开。结果发现烧杯中的水进入到广口瓶中。
③待烧杯中的水不能再进入广口瓶后,打开广口瓶的橡胶塞,将广口瓶中的水全部倒入到l00mL量筒中,测得其中水的体积为76mL。
④该同学又设法准确地测定了广口瓶中空气的体积,数据为400mL。
(1)回答下列问题:(1)红磷燃烧时最明显的现象是_____写出反应的文字表达式_____
(2)该同学测得的空气中氧气的体积分数为_____%,与理论值21%相比较 ,产生误差的原因很可能是_____(导气管的体积可忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com