铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.
问题一:硫酸铜溶液的配制
小明同学在实验室配制硫酸铜溶液时意外地发现有时会出现少量白色浑浊,对此,他和化学兴趣小组同学作出如下探究.
| 配置用水 | 有浑浊 | 有浑浊 |
| 自来水 | 无浑浊 | 有浑浊 |
| 市售纯净水 | 无浑浊 | 有浑浊 |
| 医用纯净水 | 无浑浊 | 无浑浊 |
| 试验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 饱和溶液 | 2 | 4 | 6 | 8 | 16 | 32 | 128 |
| 现 象 | 白色浑浊→澄清 |
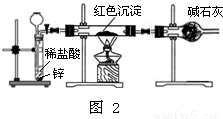
图 1
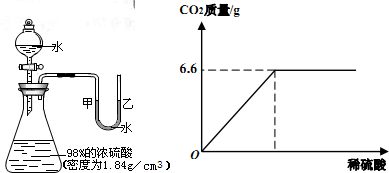
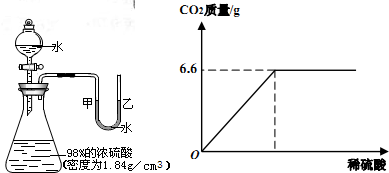
(1)形成浑浊条件分析:小明分别作出如图1配制方式,并记录现象如下:
另外,他将配好的饱和且澄清的硫酸铜溶液滴入纯净水中有如上现象,在配制过程中形成白色浑浊的因素可能有______、______、______等,因此,在实验室配制硫酸铜溶液时要用的配制用水是______ (选填“自来水、市售纯净水、医用蒸馏水”)、在______(选填“较低温度、较高温度”)下配制稍浓些的硫酸铜溶液.
(2)白色浑浊成分分析.
[查阅资料]同学们上网查阅资料获知:此白色沉淀是一种名为碱式硫酸铜的物质,它可溶于酸,其有多种可能的组成,如Cu
2(OH)
2SO
4、Cu
3(OH)
4SO
4或Cu
4(OH)
6SO
4等.为确定此次得到的白色沉淀究竟是哪种组成,小明设计实验如下:
[设计实验]称取5.16g白色沉淀,分成两等份:一份溶于足量的 中,向溶液中滴加足量的氯化钡溶液,过滤、洗涤、干燥,得2.33g白色固体;将另一份固体在空气中充分灼烧得到黑色固体1.60g.
[得出结论]通过计算确定该白色沉淀中Cu
2+、OH
-、SO
42-的质量比为______,其化学式为______. (写出计算过程,共4分)
问题二:氢氧化铜与葡萄糖反应产物的分析
利用新制氢氧化铜可以验证葡萄糖的存在.下面是三个研究性学习小组分别从不同层面对此实验开展的研究性学习活动:
Ⅰ.研究性学习小组甲对教材实验结论葡萄糖与新制氢氧化铜反应生成的红色沉淀是Cu2O,提出质疑,他们认为红色沉淀不一定是氧化亚铜.为了确定红色沉淀的成分,开展了如下研究:
提出猜想:红色沉淀可能是______、______或二者混合物.
查阅资料:①氧化亚铜能与酸反应,得到+2价的铜离子和单质铜;②在空气中灼烧氧化亚铜生成氧化铜;③铜能与稀硝酸反应生成硝酸铜、水和一氧化氮.
设计方案:方案1:取该红色沉淀溶于足量的稀硝酸中,观察溶液颜色变化;
方案2:取该红色沉淀溶于足量的稀硫酸中,观察是否有残渣;
方案3:称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器里冷却,再称重,反复多次直到固体恒重,称得质量为b g,比较a、b关系;
你认为合理的方案是______.
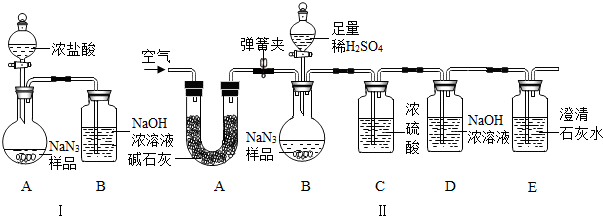
Ⅱ.研究性学习小组乙针对小组甲的质疑,设计新的探究方案,装置如图2所示.
①通入氢气体积 ②反应前,红色沉淀+硬质玻璃管的总质量
③完全反应后,红色固体+硬质玻璃管的总质量 ④实验前,干燥管(含其中固体)质量
⑤硬质玻璃管质量 ⑥锌粒质量 ⑦稀硫酸中含溶质的量 ⑧实验后,干燥管(含其中固体)质量 (已知氢气在加热条件下能与金属氧化物发生置换反应,且假设反应能完全进行)
A.②④⑤⑧B.②③⑤C.①⑥⑦D.①②⑤
你认为需要测定上述______ (选择正确的字母填空)即可确定上述红色沉淀成分.
Ⅲ.研究性学习小组丙上网查阅得知,“2005年诺贝尔化学奖授予了三位研究绿色化学的科学家”.绿色化学强调对环境友好,实现零排放.“变废为宝”符合绿色化学要求.他们收集上述红色沉淀制备化学试剂--胆矾.他们设计了一个简单且符合绿色化学要求的实验方案:将红色固体反复灼烧后,用足量稀硫酸溶解,再将所得溶液蒸发结晶,减压过滤,用少量95%的酒精淋洗晶体,晾干或用滤纸吸干.晶体用酒精淋洗而不用水洗的好处是:______.

 铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.
铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.