
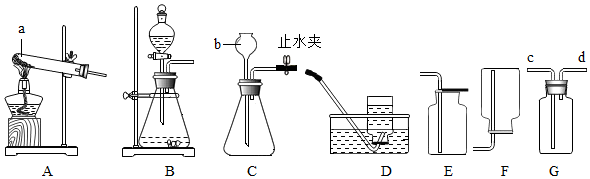

分析 (1)根据实验室常用仪器解答;
(2)根据如果用双氧水和二氧化锰制氧气就不需要加热,二氧化锰起催化作用;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净解答;
(3)根据用高锰酸钾制氧气就需要加热,试管口要放一团棉花,防止高锰酸钾粉末进入导管解答;
(4)根据铁丝在氧气中燃烧的现象以及注意事项进行分析解答即可;
(5)根据实验室制取甲烷的反应原理和甲烷的性质选择所需装置.
解答 解:
(1)根据实验室常用仪器可知:a试管;b长颈漏斗;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,二氧化锰起催化作用;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;该反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;若选用B装置来制取氧气,与C装置相比其优点是可以控制反应的发生和停止;
(3)如果用高锰酸钾制氧气就需要加热,试管口要放一团棉花,防止高锰酸钾粉末进入导管;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,故答案为:试管口放一团棉花;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(4)a.螺旋状铁丝的末端系一根火柴的作用是引燃;
b.若实验过程中没有观察到铁丝燃烧的现象,可能的原因是 氧气不纯(铁丝表面有生锈等);
c.由于反应中生成了高温熔融物,需要在集气瓶底部放少量的水或细沙,防止炸裂瓶底;
(5)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于“固固加热型”,所以应选择的发生装置为 A,甲烷密度小于空气,难溶于水,可选择向下排空气法或排水法收集,所以选择收集装置为D或F.
故答案为:
(1)a试管;b长颈漏斗;
(2)D;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;可以控制反应的发生和停止;
(3)试管口要放一团棉花;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
(4)a引燃;b氧气不纯(铁丝表面有生锈等);c集气瓶没有防水或细沙;
(5)A;DF.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 试管中液体体积不能超过试管容积的$\frac{2}{3}$ | |
| B. | 试管夹夹在距试管口的$\frac{1}{3}$处 | |
| C. | 用50mL量筒量取40.25mL水 | |
| D. | 用托盘天平称量5.02g的食盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A~I是初中化学常见的物质,它们之间的相互关系如图所示,(“→”指向生成物.)其中B是红色粉末,A、C常温下是气体,H和I中含有一种相同元素,H不溶于稀硝酸.请回答下面问题:
A~I是初中化学常见的物质,它们之间的相互关系如图所示,(“→”指向生成物.)其中B是红色粉末,A、C常温下是气体,H和I中含有一种相同元素,H不溶于稀硝酸.请回答下面问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | T<-196℃ | B. | T>-183℃ | C. | -196℃<T<-183℃ | D. | T=0℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象 | 果肉表面不变色 |
| 猜想② | 果肉表面变色 | |
| 猜想③ | 果肉表面不变色 | |
| 猜想④ | 果肉表面不变色 | |
| 猜想⑤ | 温度高的先变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com