
【题目】如图是 a、b、c 三种物质的溶解度曲线。
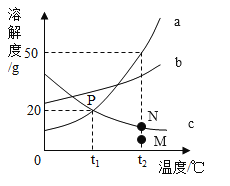
(1)点 P 表示____________;
(2)要使 M 点的 c 溶液变成 N 点的 Cc溶液,可采取的一种措施是__________;
(3)当 a 中含有少量的 b,要得到纯净的 a,可采用的方法是_____________;
(4)t2℃时,等质量的 a、b、c 三种物质的饱和溶液降温到 t1℃时,三种溶液的质量分数由大到小的顺序_________;
(5)t2℃时,75g a 物质的饱和溶液降温到 t1℃,析出 a 物质____________g。
【答案】t1℃时,a、c的溶解度相等,为20g 增加c物质或蒸发溶剂 降温结晶 b>a>c 15g
【解析】
(1)t1℃时,a、c的溶解度曲线相交,说明t1℃时,a、c的溶解度相等,故P点表示:t1℃时,a、c的溶解度相等,为20g;
(2)M 点的c溶液为不饱和溶液,N点为相同温度下c的溶液为饱和溶液,故要使M点的c溶液变成N点的c溶液,可采取增加c物质、蒸发溶剂的措施;
(3)a的溶解度受温度的影响较大,b的溶解度受温度的影响较小,故当 a 中含有少量的 b,要得到纯净的 a,可采用的方法是:降温结晶;
(4)a、b的溶解度随温度的升高而增加,c的溶解度随温度的升高而减小,故t2℃时,将等质量的 a、b、c 三种物质的饱和溶液降温到 t1℃时,a、b还是饱和溶液,c变为不饱和溶液,降温后,c的溶质质量分数不变,t1℃时,b的溶解度大于该温度下a的溶解度大于t2℃时,c的溶解度,故t1℃时,b的饱和溶液的溶质质量分数大于该温度下,a的饱和溶液的溶质质量分数,大于t2℃时,c的饱和溶液的溶质质量分数,故t2℃时,等质量的 a、b、c 三种物质的饱和溶液降温到 t1℃时,三种溶液的质量分数由大到小的顺序:b>a>c;
(5)t2℃时,a的溶解度为50g,75g a 物质的饱和溶液中含a物质的质量为:![]() ,溶液中水的质量为:75g-25g=50g,t1℃时,a的溶解度为20g,50g水只能溶解10ga物质,故析出a物质的质量为:25g-10g=15g。
,溶液中水的质量为:75g-25g=50g,t1℃时,a的溶解度为20g,50g水只能溶解10ga物质,故析出a物质的质量为:25g-10g=15g。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:初中化学 来源: 题型:
【题目】碳酸锶(SrCO3)可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO3和NaCl固体混合物中SrCO3的质量分数,在三个烧杯中进行相关实验,实验所用稀盐酸的溶质的质量分数相同。所得数据如下表所示:
烧杯编号 | ① | ② | ③ |
稀盐酸质量/g | 100 | 200 | 300 |
固体混合物质量/g | 100 | 100 | 100 |
反应后烧杯中物质的质量/g | 195.6 | 291.2 | 391.2 |
试求:
(1)烧杯②中产生CO2的质量为____g。
(2)原固体混合物中SrCO3的质量分数____(计算结果精确到0.1%)。
(提示:SrCO3+2HCl===SrCl2+CO2↑+H2O)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像关系合理的是( )
A.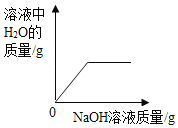 向一定量稀盐酸中加入氢氧化钠溶液
向一定量稀盐酸中加入氢氧化钠溶液
B.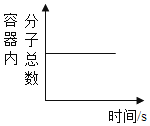 甲烷和足量的氧气在密闭容器中完全反应
甲烷和足量的氧气在密闭容器中完全反应
C.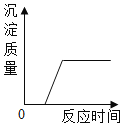 往Na2SO4和HC1的混合溶液中加入Ba(OH)2溶液
往Na2SO4和HC1的混合溶液中加入Ba(OH)2溶液
D.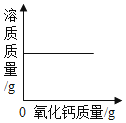 向一定量饱和的石灰水中加氧化钙
向一定量饱和的石灰水中加氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】袋装食品中常用一种“双吸剂”保持,主要成分是铁粉和生石灰,同学们对一久置的双吸剂固体样品很好奇,设计了如下实验进行探究.
【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有_______.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
实验操作 | 实验现象 | 实验结论 |
取少量探究实验1的残留固体放入试管中,加入蒸馏水。 | 试管外壁不发烫 | 固体中一定没有 _____________ |
【实验探究3】
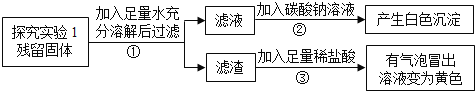
【实验结论】
(1)步骤②产生白色沉淀,说明久置的“双吸剂”中含有_________,其反应的化学方程式:___________________。
(2)步骤③有气泡冒出,溶液变为黄色,说明久置的“双吸剂”中含有_______和______。所涉及的两个反应的化学方程式为:_______________;_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A- H均为初中化学常见的物质。其中A、C常温下是气体,且组成元素相同,B是赤铁矿的主要成分,E能用于改良酸性土壤,H是紫红色单质,F含有两种元素。他们的相互转化关系如图所示(图中反应条件均已略去)。请回答下列问题:

(1)写出E物质的俗称______________。
(2)写出反应①的化学方程式______________。
(3)F与某物质反应可生成白色沉淀,写出该反应的化学方程式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的两个实验:
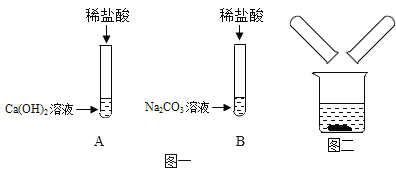
(1)写出 B 试管中反应的化学方程式___________;
(2)实验结束后,小组同学将 A、B 两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示), 观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成 分进行探究:
(作出猜想)
甲同学猜想:NaCl
乙同学猜想:NaCl、CaCl2、HCl
丙同学猜想:NaCl、CaCl2
丁的猜想是:_____________
(查阅资料)NaCl、CaCl2 溶液均呈中性。
(交流讨论)
甲同学认为_____________同学的猜想一定不正确,理由是:______________;
(设计实验)丙、丁两位同学分别设计如下实验验证自己的猜想:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
丙 | 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想正确 |
丁 | 取少量滤液于试管中,向其中滴加适量稀盐酸 | _____ | 猜想正确 |
(反思评价)
实验结束后,甲同学认为_____(填“丙”或“丁”)同学的实验结论是错误的,理由是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某一批次盐酸的溶质质量分数,取其中一瓶和一定量的锌粒进行了如下实验(不计每步损耗)。
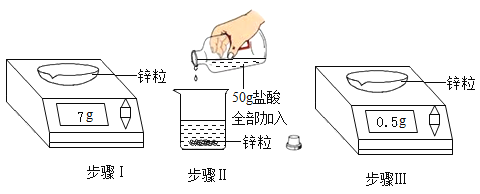
步骤 I :称取一定质量锌粒7g。
步骤 II:将 I 称量所得锌粒转移至烧杯中,加入该50g盐酸充分反应。
步骤 III:将 II 中反应后的混合物过滤,对剩余锌粒烘干、冷却再称量0.5g。
①参加反应的锌粒的质量是___________________,物质的量为___________________mol。
②该盐酸溶质质量分数(根据化学方程式列式计算)___________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】农药在农业生产上起着重要的作用。目前市售蔬菜农药残留量虽然已达到国家标准,我们可选择科学的清洗方法,更好降低食用蔬菜的农药残留量。果果分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
(1)清洗方法一:清水浸泡。图1呈现出两种农药的去除率随浸泡时间的变化。

(2)洗洁精清洗。实验选择了6种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到 60%以上,最高可达到 84%。
(3)碱性溶液浸泡。食用碱(Na2CO3和NaHCO3)溶液有利于农药分解。 图2表示不同浓度的食用碱溶液对农药去除率的影响。
①依据图 1 分析,去除农药残留的最佳浸泡时间是_____ min。洗洁精
②食用碱中的NaHCO3俗称为_____,食用碱溶液的 pH_____(填“>”“<”或“=”)7。
③依据图 2分析,用食用碱溶液浸泡含有农药甲的蔬菜时,要想超过清水浸泡的最大去除率,可以选取的浓度_____(填序号)
A 2% B 8% C 10% D 15%
④下列有关蔬菜清洗方法的说法中正确的是_____(填序号)
A 采用清水浸泡去除农药的时间不宜过长
B 多数洗洁精对农药的清洗效果比清水浸泡的好
C 食用碱的去除效果较好,是因为在浸泡过程中农药发生了化学变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素被誉为“抗癌大王”。硒元素在元素周期表中的部分信息如图所示,下列说法中不正确的是( )
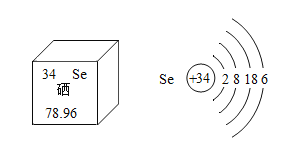
A.硒元素的相对原子质量为78.96B.一个硒原子中有34个中子
C.硒原子结构示意图中的X=18D.硒元素在化合物中可能显-2价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com