


| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
 =
=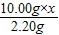 ,
,

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
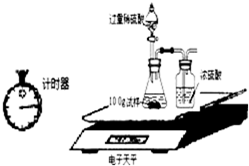
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
查看答案和解析>>
科目:初中化学 来源:2012届江苏省无锡市省锡中九年级3月反馈练习化学试卷(带解析) 题型:探究题
(11分)小刚、小军、小红对一久置的NaOH白色粉末的成分进行探究并测定其成分的含量。
(一)成分的确定
三位同学都作出以下的猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH与Na2CO3的混合物.做出②③猜想的依据是 (化学方程式表示)。
为了验证①②③猜想,他们分别做了下面的实验。
(1)小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有 ,肯定猜想 (填序号)是错误的。
(2)小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军结合小刚的实验,认为猜想③是正确的.小红却认为小军的所得结论不确切,因为 。
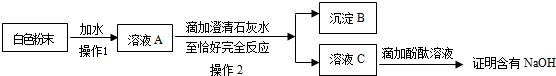
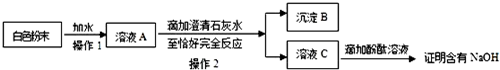
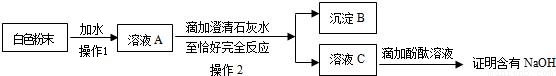
(3)为探究白色粉末是否含有NaOH,小红设计了如下实验方案: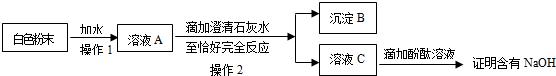
①沉淀B的化学式为 ;在操作1中要用到玻璃棒,其作用是 。
②小刚认为小红的这个方案也有问题,理由是 。但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是 。小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③是正确的。
二、各成分含量的测定
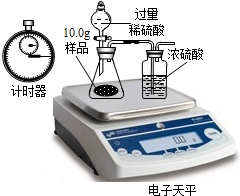
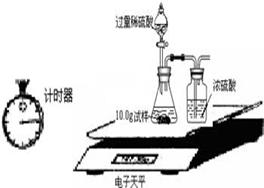
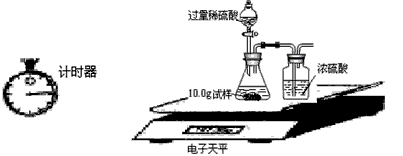
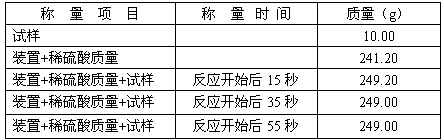
三位同学利用电子天平共同作了以下测定实验.实验数据记录如下:
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | | 10.00 |
| 装置+稀硫酸质量 | | 241.20 |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
查看答案和解析>>
科目:初中化学 来源:江苏省期末题 题型:实验题
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省无锡市省锡中实验学校九年级化学反馈练习卷(3月份)(解析版) 题型:解答题

| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com