
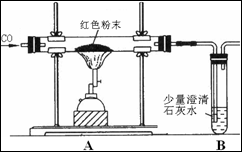
| | 反应前 | 反应后 |
| 方法1 | 玻璃管和红色粉末的总质量为37.3 g | 玻璃管和固体物质的总质量为36.1 g |
| 方法2 | 洗气瓶和所盛溶液的总质量为180.0 g | 洗气瓶和瓶中物质的总质量为183.1 g |


科目:初中化学 来源:不详 题型:实验题
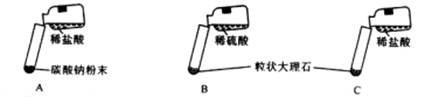
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止。 | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ① | ② |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
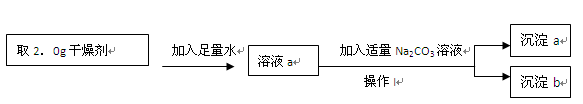
| A.称取2.0g干燥剂要用到的仪器是托盘天平 |
| B.操作I是过滤 |
| C.溶液a与溶液b可能都含有OH-且具有相似的性质 |
| D.该干燥剂的主要成分可能是生石灰,也可能是烧碱 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
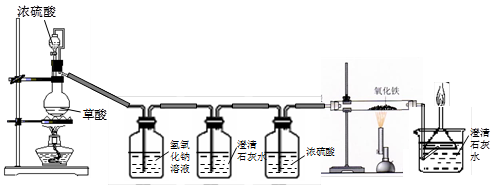
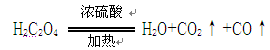 。请回答下列问题:
。请回答下列问题: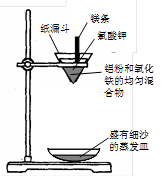
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 黑色粉末变成 色 固体部分溶解,有气泡产生,水溶液呈无色。 | Zn和CuO能发生置换反应。 |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 发生爆炸,黑色粉末变成红色。 固体部分溶解,有气泡产生,水溶液呈 色。 | |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热。 | 粉末无变化 | Cu、Fe2O3不能反应。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
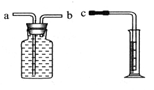

| | 实验方案 | 实验现象 | 实验结论 |
| 方 案 一 | 将Fe丝浸入CuSO4溶液中 | Fe丝表面有红色物质析出 | 金属活动性:Fe_ _Cu(填“>”或“<”)该反应的反应类型属于 ____________反应。 |
| 方 案 二 | 将Mg和Cu分别在空气中灼烧 | 发现镁能剧烈燃烧,而另一种不能 | 金属活动性:Mg_ _Cu(填“>”或“<”) |
| 方 案 三 | 分别将Mg和Fe放入_________中,观察现象 | 观察到_ (填元素符号)产生气泡的速度较慢 | 金属活动性顺序:Mg>Fe |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| | 实验一 | 实验二 | 实验三 |
| 实验方案 | 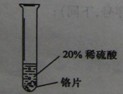 | 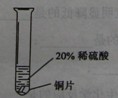 | 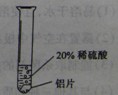 |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变蓝色 | 无明显现象 | 铝片表面产生气泡较快 |
| 结论 | 铬能与稀硫酸发生反应,反应速率较慢 | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com