
| A. | 过滤 | B. | 沉淀 | C. | 吸附 | D. | 蒸馏 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
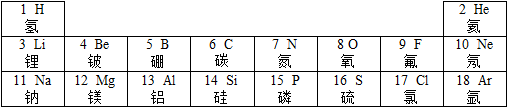
 元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.如表是元素周期表部分内容(元素原子结构示意图已给出),请回答下列问题.
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.如表是元素周期表部分内容(元素原子结构示意图已给出),请回答下列问题.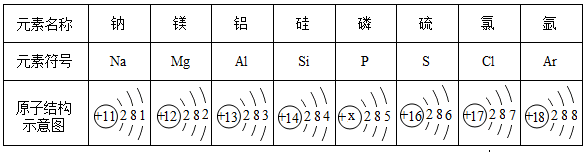 (1)在元素周期表中,原子序数为12的元素符号是Mg,其原子结构示意图如图所示,在化学反应中该原子容易失去(填“得到”或“失去”)电子,形成的离子符号为Mg2+;
(1)在元素周期表中,原子序数为12的元素符号是Mg,其原子结构示意图如图所示,在化学反应中该原子容易失去(填“得到”或“失去”)电子,形成的离子符号为Mg2+;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu(OH)2的相对分子质量:64+(16+1)×2═98 | |
| B. | SO2中硫元素与氧元素的质量比为32:(16×2)=1:1 | |
| C. | NH3NO3中氮元素的质量分数为$\frac{14}{80}$×100%=17.5% | |
| D. | 18g水中含氢元素的质量为18g×$\frac{1×2}{18}$×100%=2g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 铜在工农业生产中应用广泛.请回答:
铜在工农业生产中应用广泛.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com