
【题目】以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:

已知“沉淀”时的主要反应为:![]()
(1)FeO(OH)中铁元素的化合价为_______。FeO(OH)可表示为mFe2O3·nFe(OH)3,![]() =_____________。
=_____________。
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有__________(填字母)。
A 能与酸反应
B 能与碱反应
C 不与FeO(OH)反应
②“沉淀”时反应温度不宜过高,其原因是_______。
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为__________(填离子符号)。
(4)“煅烧”时反应的化学方程式为________。
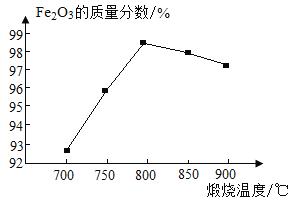
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是___________。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是_______。
(6)用该方法制备Fe2O3,计算理论上13.9 t FeSO4·7H2O(相对分子质量为278)可制得Fe2O3的质量(写出计算过程)。_________。
【答案】+3 1 AC 温度过高会导致过氧化氢挥发,不利于反应的进行 SO42- 2FeO(OH)![]() Fe2O3+ H2O 低温条件下FeO(OH)不易分解 生成了四氧化三铁或氧化亚铁 4t
Fe2O3+ H2O 低温条件下FeO(OH)不易分解 生成了四氧化三铁或氧化亚铁 4t
【解析】
(1)化合物中元素的化合价代数和为零,设FeO(OH)中铁元素的化合价为x,则x+(+1)+(-2)×2=0,x=+3,FeO(OH)可表示为mFe2O3·nFe(OH)3,FeO(OH)和mFe2O3·nFe(OH)3中原子个数比相同,则![]() ,得
,得![]() =1;
=1;
(2)已知“沉淀”时的主要反应为:![]() ,①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有:A、 能与酸反应,将生成的硫酸部分反应掉,使溶液的酸性不能太强,选项正确;
,①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有:A、 能与酸反应,将生成的硫酸部分反应掉,使溶液的酸性不能太强,选项正确;
B、不能与碱反应,选项错误;
C、不与FeO(OH)反应,否则会导致产率偏小,甚至得不到产品,选项正确;故选AC;
②“沉淀”时反应温度不宜过高,其原因是温度过高会导致反应物过氧化氢挥发,不利于反应的进行;
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的溶质是硫酸及调节酸碱性时可能产生的可溶性硫酸盐,阴离子为SO42-;
(4)根据质量守恒定律可推知,“煅烧”时反应是FeO(OH)在高温条件下分解生成氧化铁和水,化学方程式为2FeO(OH)![]() Fe2O3+ H2O;
Fe2O3+ H2O;
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是低温条件下FeO(OH)不易分解。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是生成了四氧化三铁或氧化亚铁,因铁的氧化物有氧化亚铁,四氧化三铁,氧化铁三种,其中氧化亚铁,四氧化三铁都是黑色固体,且铁元素的质量分数比氧化铁中高;
(6)用该方法制备Fe2O3,设13.9 t FeSO4·7H2O(相对分子质量为278)理论上可制得Fe2O3的质量为x,据反应前后元素的种类、质量不变,则:13.9 t×![]() =
=![]() x, x=4t。
x, x=4t。


科目:初中化学 来源: 题型:
【题目】下列表中的叙述,对应的化学方程式和所属反应基本类型都正确的是( )
选项 | 叙述 | 化学反应方程式 | 反应类型 |
A | 电解水 |
| 分解反应 |
B | 探究一氧化碳的还原性 |
| 置换反应 |
C | 酸雨形成的原因 |
| 化合反应 |
D | 硫酸铜溶液中滴加氢氧化钠溶液 |
| 复分解反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一瓶敞口放置的氢氧化钠固体,同学们想探究其是否变质,请你一同参与并回答有关问题。
(1)写出氢氧化钠在空气中变质的化学反应方程式___________________________。
(提出猜想)
猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分是_________;
猜想3:这瓶固体的成分是NaOH和Na2CO3的混合物。
(查阅资料)①Na2CO3+HCl=NaCl +NaHCO3;NaHCO3+HCl=NaCl +CO2↑+H2O;②BaCl2溶液呈中性;③酸与碱和盐共同反应时,酸碱中和反应优先进行。
(实验与探讨)
取少量样品于烧杯中,加入适量蒸馏水,振荡,样品全部溶解。
(2)取少量溶液于试管中,向其中加入无色酚酞溶液,溶液由无色变为红色。甲同学认为猜想1正确。乙同学认为甲同学的结论不正确,其理由是_____________________。
(3)向(2)溶液中加入过量的BaCl2溶液,若有________________现象,则猜想3正确。发生反应的化学方程式为_________________。
(4)丙同学另取少量溶液于试管中,加入少量稀盐酸,没有看到气泡产生,错误地排除了猜想2和猜想3,若猜想2或猜想3正确,加入稀盐酸发生反应的化学方程式分别为_________;___________。
(深入讨论)
(5)丁同学认为BaCl2溶液也可以用Ba(OH)2溶液替代进行实验,同学们一致认为丁同学的做法是错误的,其错误的理由是___________________________________________。
(6)通过氢氧化钠变质的研究可知,凡吸收空气中的H2O、O2或CO2等物质能够变质的药品必须密封保存,请列举另一类需要密封保存的药品的例子,如_______________________。
(7)取9.3g部分变质的NaOH样品,加入足量的水配成溶液,往溶液中不断加入7.3%的稀盐酸,实验中加入稀盐酸与生成气体的质量关系如图所示:
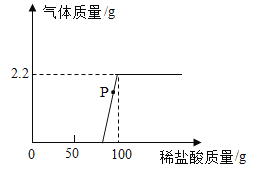
①P点溶液中溶质的成分是_______________(写化学式);
②该样品的变质率为_________(变质的NaOH与原NaOH的质量百分比)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示进行碳的氧化物的性质实验,请回答下列问题。
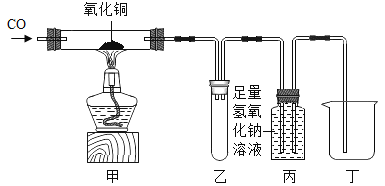
(1)甲处的实验现象为_________,发生的化学反应方程式为_______。
(2)乙装置的作用是防止液体倒吸,丙装置的作用是_______,发生的化学反应方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定质量的CH4可与常见物质M反应,同时放出少量热量;将所得产物Cu2O与O2反应又生成M,同时放出较多热量。其反应原理如下图所示。下列说法正确的是

A.M中铜元素的质量分数比Cu2O中的高
B.理论上反应每生成44gCO2,同时生成18gH2O
C.理论上每16gCH4参与反应,最终消耗64gO2
D.过程①可将CH4中的部分能量储存于Cu2O中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据信息回答下列问题:
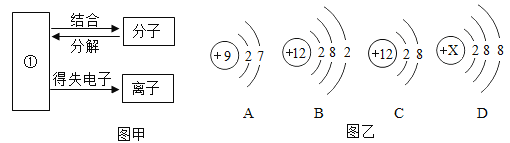
(1)图甲为粒子之间的转化关系图,其中①表示的是_____。
(2)图乙中D为某粒子的结构示意图,当X=___时,该粒子是原子。
(3)图乙中B、C属于同种元素,因为___相同。
(4)由A、B形成的化合物的化学式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用氮气合成氨气(NH3),用氨气生产硝酸,相关反应如下:
① ②
②
③![]() ④
④![]()
下列说法不正确的是
A.反应①③属于化合反应
B.反应②中 X 的化学式为 N2
C.反应④中氮元素的化合价既有升高又有降低
D.NO 和 NO2 可以相互转化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CuO是某种无机胶黏剂的组分之一,制备的部分流程如下图。
已知:CuO难溶于水。
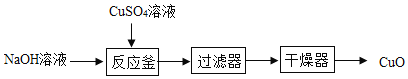
(1)反应釜中发生的反应有:①![]()
②![]() ,其中属于复分解反应的是____(填“①”或“②”)。
,其中属于复分解反应的是____(填“①”或“②”)。
(2)过滤器分离出的滤液中一定含有的溶质是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com