
| A. | 爆炸 | B. | 吸附 | C. | 升华 | D. | 燃烧 |
科目:初中化学 来源: 题型:解答题
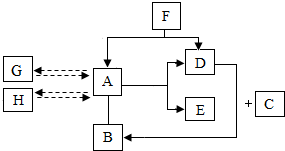 自然界中存在着氧循环、碳循环、水循环等.如图所示,其中A、G、H就是这些循环中的一种化合物在自然界中的三种存在状态,A常温下为液态;B是空气的成分之一;C是一种黑色固体单质,能燃烧;D具有助燃性和氧化性,能与许多物质发生剧烈地或缓慢地氧化反应,E是一种清洁高效的能源,其中“→”表示能生成这种物质,“-”表示两种物质间能发生化学反应.请回答下列问题:
自然界中存在着氧循环、碳循环、水循环等.如图所示,其中A、G、H就是这些循环中的一种化合物在自然界中的三种存在状态,A常温下为液态;B是空气的成分之一;C是一种黑色固体单质,能燃烧;D具有助燃性和氧化性,能与许多物质发生剧烈地或缓慢地氧化反应,E是一种清洁高效的能源,其中“→”表示能生成这种物质,“-”表示两种物质间能发生化学反应.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 构成:二氧化碳比一氧化碳多1个氧原子 | |
| B. | 性质:CO2能溶于水;CO难溶于水 | |
| C. | 用途:CO2可用于灭火;CO可作气体燃料 | |
| D. | 危害:CO2过多会造成“温室效应”加剧;CO易与血液中的血红蛋白结合引起中毒 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeCl3 NaCl KNO3 | B. | NaCl NaOH NaNO3 | ||
| C. | CaCl2 NaNO3 Na2CO3 | D. | KNO3 H2SO4 NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水蒸发变成水蒸气 | B. | 将胆矾晶体研磨变细 | ||
| C. | 氧化汞分解得到汞和氧气 | D. | 将空气加压降温变为液态空气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 加热时间(min) | 0 | T1 | T2 | T3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com