菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结石。某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(CaC2O4)。
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】“菠菜豆腐不能同食”的原因可能是_______________________。
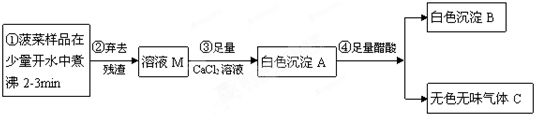
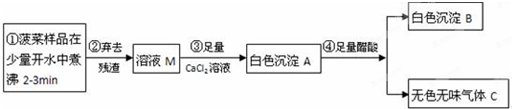
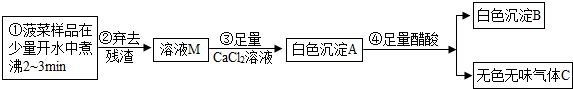
【探究一】菠菜中部分成分分析
(1)步骤③中加入足量的CaCl2溶液的目的______________________。
(2)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAc表示,写出步骤④的化学反应方程式_______________。沉淀A、B的质量关系为:m(A)_________m(B)(填“>”、“<”或“=”)。
(3)白色沉淀B的化学式为___________,由此可见菠菜豆腐不能同食。以下饮食观点正确的是__________(填字母)。
A.禁吃菠菜 B.高钙牛奶可与菠菜同食 C.菠菜烹饪时用开水烫,可降低草酸盐含量
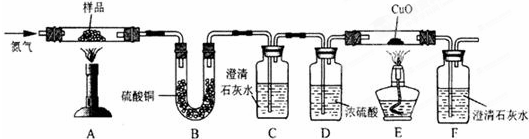
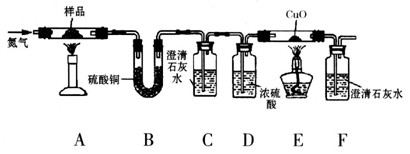
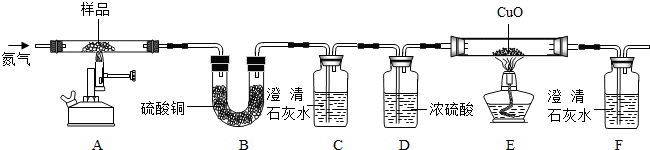
【探究二】某草酸钙晶体(CaC2O4·xH2O)热分解研究按下图装置将某草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)。
(4)①反应开始前通入氮气的目的是_______________。
②装置B中硫酸铜粉末变蓝,说明产物中有________,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物还有________和_________,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议___________________。
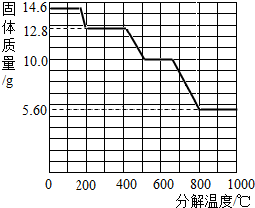
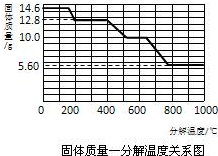
(5)某研究所利用SDTQ600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得相关数据,绘制成固体质量一分解温度的关系图(如下图)。
①800℃以上时,固体成分的化学式为_________。
②计算CaC2O4·xH2O中的x(写出计算过程,CaC2O4的相对分子质量:128)。
③残留固体为CaC2O4时的温度范围____,写出固体质量由12.8g变为10.0g时的化学方程式________________。



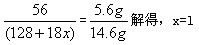
 CO2↑+CaO+CO↑+xH2O
CO2↑+CaO+CO↑+xH2O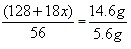
 CO↑+CaCO3
CO↑+CaCO3

 阅读快车系列答案
阅读快车系列答案
 (4)①反应开始前通入氮气的目的是
(4)①反应开始前通入氮气的目的是