
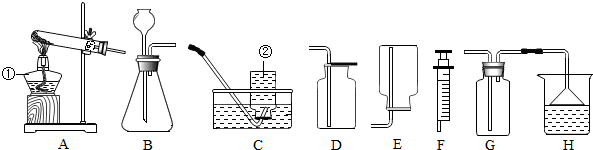
·ÖĪö £Ø1£©ŌŚŹµŃéŹŅĢõ¼žĻĀ£¬ĄūÓĆŹ³ŃĪ¾§ĢåÅäÖĘČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĀČ»ÆÄĘČÜŅŗ£¬Ņ»°ćŅŖ¾¹żĖÄøö²½Öč£ŗ¼ĘĖćĖłŠčµÄČÜÖŹÖŹĮæŗĶČܼĮĢå»ż£»³ĘĮæŗĶĮæČ”ĖłŠčµÄČÜÖŹŗĶČܼĮ£»°ŃČÜÖŹČܽāŌŚČܼĮÖŠ£»°ŃÅäÖĘŗƵÄČÜŅŗ×°ČėŹŌ¼ĮĘæÖŠ£¬ČūŗĆĘæČū£¬ĢłŗƱźĒ©£¬·ÅČėŹŌ¼Į¹ńÖŠ£®
£Ø2£©ŌŚÅäÖĘČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ10%µÄĀČ»ÆÄĘČÜŅŗ¹ż³ĢÖŠ£¬ĪŅĆĒ¾ĶŅŖÓƵ½ĻąÓ¦µÄŹµŃéŅĒĘ÷ŗĶŅ©Ę·£®³ĘĮæŹ³ŃĪ¾§ĢåŠčŅŖÓƵ½ĶŠÅĢĢģĘ½£»ĮæČ”ČܼĮĄė²»æŖĮæĶ²£»°ŃČÜÖŹČܽāŌŚČܼĮÖŠŠčŅŖÉÕ±£¬²¢ÓĆ²£Į§°ōĒįĒį½ĮŌČČÜŅŗ£®ĮķĶā£¬»¹ŅŖ°ŃÅäÖĘŗƵÄČÜŅŗ×°ČėŹŌ¼ĮĘæÖŠ£¬ČūŗĆĘæČū£¬ĢłŗƱźĒ©£¬·ÅČėŹŌ¼Į¹ńÖŠ£®
£Ø3£©ČōČÜÖŹÖŹĮæĘ«Š”£¬½«µ¼ÖĀČÜÖŹÖŹĮæ·ÖŹżĘ«Š”£»ČōČܼĮÖŹĮæĘ«“óŅ²»įµ¼ÖĀČÜÖŹÖŹĮæ·ÖŹżĘ«Š”£®¾Ż“Ė»Ų“š£®
½ā“š ½ā£ŗ£Ø1£©ŹµŃéŹŅÅäÖĘČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ10%µÄĀČ»ÆÄĘČÜŅŗ£¬ŠčŅŖµÄ²Ł×÷²½ÖčŹĒ¼ĘĖć”¢³ĘĮ攢ĮæČ”ŗĶČܽā£®
£Ø2£©ĮæČ”ÕōĮóĖ®ŅŖÓƵ½µÄÖ÷ŅŖŅĒĘ÷ŹĒĮæĶ²£®
£Ø3£©A£®ĀČ»ÆÄĘ¹ĢĢåÖŠŗ¬ÓŠŌÓÖŹ£¬Ōģ³ÉČÜÖŹÉŁĮĖ£¬½«µ¼ÖĀČÜÖŹÖŹĮæ·ÖŹżĘ«Š”£»
B£®¹ĢĢåµ¹ČėÉÕ±Ź±Č÷Ā䣬Ōģ³ÉČÜÖŹÉŁĮĖ£¬½«µ¼ÖĀČÜÖŹÖŹĮæ·ÖŹżĘ«Š”£»
C£®ÅäÖĘŹ±ÉÕ±²»øÉŌļ£¬Ōģ³ÉČܼĮÖŹĮæĘ«“󣬽«µ¼ÖĀČÜÖŹÖŹĮæ·ÖŹżĘ«Š”£»
D£®×°ĘæŹ±ÓŠŅŗĢ彦³ö£¬ČÜÖŹÖŹĮæ·ÖŹżĪŽÓ°Ļģ£»
ĖłŅŌŹµ¼ŹÅäÖʵÄČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżŠ”ÓŚ10%£¬ĘäŌŅņæÉÄÜÓŠABC£®
¹Ź“š°øĪŖ£ŗ
£Ø1£©Čܽā£»
£Ø2£©ĮæĶ²£»
£Ø3£©ABC£®
µćĘĄ ŹµŃ鏱£¬Ņ»¶ØŅŖĮĖ½āŗĶČĻŹ¶»ÆѧŹµŃéŹŅÖŠµÄø÷ÖÖÉč±ø”¢ŅĒĘ÷ŗĶŅ©Ę·£®±¾ĢāÖ÷ŅŖæ¼²é·ÖĪöŹµŃé¹ż³ĢµÄÄÜĮ¦£¬Ņņ“ĖÕżČ·µÄ·ÖĪö”¢½āŹĶŹµŃé¹ż³ĢŹĒѧɜӦøĆ¾ß±øµÄŅ»ÖÖÄÜĮ¦£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°¾ĘĻć²»ÅĀĻļ×ÓÉī”±ĖµĆ÷·Ö×ÓŹĒ²»¶ĻŌĖ¶ÆµÄ | |
| B£® | ·Ö×ÓŹĒ±£³ÖĪļÖŹŠŌÖŹµÄ×īŠ”Į£×Ó | |
| C£® | Ō×ÓŹĒ»Æѧ±ä»ÆÖŠµÄ×īŠ”Į£×Ó | |
| D£® | ·Ö×ÓæÉŅŌ»Æ·Ö³ÉŌ×Ó£¬Ō×ÓæÉŅŌ¹¹³É·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żĮ×ĖįøĘ | B£® | ÄņĖŲ | C£® | ĻõĖįļ§ | D£® | ĀČ»Æ¼Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃõĘųÓĆÓŚĮ¶øÖ | B£® | øɱłÓĆÓŚČĖ¹¤½µÓź | ||
| C£® | ĮņĖįÓĆÓŚ“¦Ąķ¼īŠŌ·ĻŅŗ | D£® | Ģś·ŪÓĆ×÷Ź³Ę·±£ĻŹĪüŃõ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ”¾Č«¹śŹŠ¼¶ĮŖæ¼”æɽ¶«Ź”ŹŁ¹āŹŠ2017½ģ¾ÅÄź¼¶Ń§ŅµĖ®Ę½Ä£Äāæ¼ŹŌ£ØŅ»Ä££©»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢ½¾æĢā
ij»Æ¹¤³§ĪŖ×ŪŗĻĄūÓĆÉś²ś¹ż³ĢÖŠµÄø±²śĘ·CaSO4¶ųÓėĻąĮŚµÄ»Æ·Ź³§ĮŖŗĻÉč¼ĘµÄÖʱø£ØNH4£©2SO4µÄ¹¤ŅÕĮ÷³Ģ”£
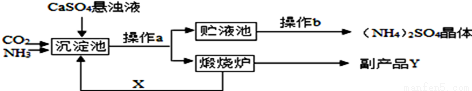
£Ø1£©²Ł×÷bµÄĆū³ĘŹĒ____________”£
£Ø2£©XŃ»·Ź¹ÓĆÓŠĄūÓŚ½ŚÄܼõÅÅ”¢½µµĶÉś²ś³É±¾£¬XŹĒ______£¬ø±²śĘ·YŹĒ________ ”£
£Ø3£©ĪŖ“Ł½ųCO2µÄČܽāĪüŹÕ£¬Ó¦ĻČĻņ³Įµķ³ŲÖŠĶØČėNH3£¬ŌŁĶØČėCO2³Įµķ³ŲÖŠ·¢ÉśµÄÖ÷ŅŖ»Æѧ·“Ó¦ĪŖ__________________________________________”£
£Ø4£©ÅŠ¶Ļ£ØNH4£©2SO4»Æ·ŹÖŠÓŠĪŽNH4HCO3µÄ·½·Ø£ŗȔɣĮæŹ½ŃłČÜÓŚĖ®£¬µĪ¼Ó×ćĮæµÄ____________£¬Čō³öĻÖ___________________________ĻÖĻó£¬ŌņæÉÅŠ¶ĻøĆ»Æ·ŹÖŠ²»“ęŌŚNH4HCO3”£
£Ø5£©“ÓĀĢÉ«»ÆѧŗĶ׏Ō“×ŪŗĻĄūÓĆµÄ½Ē¶ČĖµĆ÷ÉĻŹöĮ÷³ĢµÄÖ÷ŅŖÓŵćŹĒ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Īļ ÖŹ | Ca£ØHCO3£©2 | Mg£ØHCO3£©2 | Ca£ØOH£©2 | Mg£ØOH£©2 | CaCO3 | BaCO3 |
| ČܽāŠŌ | æÉČÜ | æÉČÜ | Ī¢ČÜ | ²»ČÜ | ²»ČÜ | ²»ČÜ |
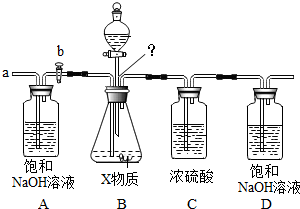
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
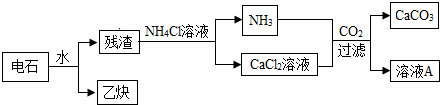
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±Ęų | B£® | ½š | C£® | Ė® | D£® | ĮņĖįĶ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com