
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)实验室制取氧气可以采用分解过氧化氢溶液的方法,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(合理即可).
(3)镁和盐酸反应生成氯化镁和氢气,反应的化学方程式为:Mg+2HCl═MgCl2+H2↑.
(4)氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
(5)天然气(主要成分是甲烷)在空气中完全燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(6)酒精(化学式C2H6O)在空气中完全燃烧生成二氧化碳和水,反应的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案为:(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(合理即可);(3)Mg+2HCl═MgCl2+H2↑;(4)Fe2O3+6HCl═2FeCl3+3H2O;(5)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(6)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
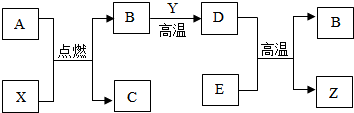
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质跟氧气的反应就是燃烧 | |
| B. | 物质在有限的空间内燃烧,可能会发生爆炸 | |
| C. | 燃烧一定有火焰 | |
| D. | 使可燃物温度降低,一定可以灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子在不停地运动 | B. | 分了之间有间隔 | ||
| C. | 同种分子的化学性质相同 | D. | 分子有一定的大小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将氢氧化钠固体、硝酸铵固体、氯化钠固体分别溶于水,就可区分它们 | |
| B. | 用紫色石蕊试液可以一次性区分Na2CO3、NaCl、H2SO4三种溶液 | |
| C. | 用通入二氧化碳的方法能区分氢氧化钠溶液和饱和石灰水 | |
| D. | 用氢氧化钡一次性区分:NaOH、MgSO4、HCl三种溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
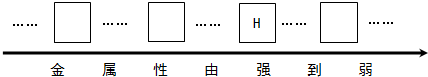
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 氯酸钾的质量 | 催化剂的种类 | MnO2的质量 | 反应条件 | 收集45.0mL O2所需的时间(S) | |
| Ⅰ | 3.0g | MnO2 | 1.0g | 混合加热 | 21 |
| Ⅱ | xg | CuO | 1.0g | 混合加热 | 48 |

| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 温度 | 相同时间(10S)内产生O2体积(mL) | |
| Ⅰ | 50.0g | 1% | 0.1g | 20℃ | 9 |
| Ⅱ | 50.0g | 2% | 0.1g | 20℃ | 16 |
| Ⅲ | 50.0g | 4% | 0.1g | 20℃ | 31 |
| 时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com