
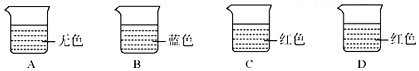
分析 (1)根据A中溶液显无色,说明A溶液显酸性,加入的指示剂是酚酞试液,能与氧化铁反应生成铁盐和水,据此分析回答有关的问题;
(2)根据碳酸钠溶液显碱性,能使酚酞试液变成红色,能与氯化钡溶液反应生成了碳酸钡白色沉淀,碳酸钡白色沉淀能溶于稀硝酸,溶液由碱性变成了中性或酸性,使酚酞试液不变色;据此分析回答;
(3)根据稀硫酸显酸性,能使石蕊试液变成红色,能与氯化钡溶液反应生成了硫酸钡沉淀,不溶于稀硝酸,据此分析回答.
(4)根据上述分析即可推出B烧杯中最初盛有的物质.
解答 解:(1)由题意可知,A中溶液显无色,说明A溶液显酸性,加入的指示剂是酚酞试液,能与氧化铁反应生成铁盐和水,所以则黄色溶液中含有的金属阳离子为Fe3+;
(2)由于碳酸钠溶液显碱性,能使酚酞试液变成红色,能与氯化钡溶液反应生成了碳酸钡白色沉淀,碳酸钡白色沉淀能溶于稀硝酸,溶液由碱性变成了中性或酸性,使酚酞试液不变色,所以C烧杯的溶液的是碳酸钠溶液,加入的指示剂是酚酞试液;
(3)由于稀硫酸显酸性,能使石蕊试液变成红色,能与氯化钡溶液反应生成了硫酸钡沉淀,该沉淀沉淀不溶于稀硝酸,所以D中的溶液是稀硫酸,与氯化钡反应的化学方程式是:H2SO4+BaCl2═BaSO4↓+2HCl;
(4)由上述分析可知,B中的溶液是饱和石灰水,能使酚酞试液变成了蓝色.
故答案为:(1)Fe3+;(2)酚酞试液;(3)H2SO4+BaCl2═BaSO4↓+2HCl;(4)饱和石灰水.
点评 本考点属于物质的推断题,是通过指示剂的变色、常见离子的检验方法,在比较鉴别的基础上,得出了正确的实验结论.本题是通过实验现象,从而得出物质的组成.此考点主要出现在填空题和实验题中.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质的方法 | |
| A | NaOH溶液 | Ca(OH)2 | 过量Na2CO3溶液,过滤 |
| B | CaCl2溶液 | HCl | 过量CaCO3,过滤 |
| C | Zn | Fe | Zn(NO3)2,过滤 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
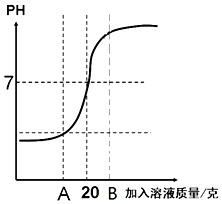 在用4%氢氧化钠溶液和溶质质量分数为4.9%的稀硫酸进行酸碱实验时,反应过程中溶液酸碱度变化及相关数据如图所示.
在用4%氢氧化钠溶液和溶质质量分数为4.9%的稀硫酸进行酸碱实验时,反应过程中溶液酸碱度变化及相关数据如图所示. 查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
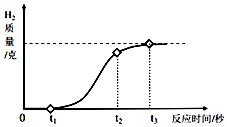 铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔.
铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2.2g | B. | 2.6g | C. | 3g | D. | 3.4g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 互为同位素原子 | |
| B. | ${\;}_{8}^{18}$O 的核外电子数多于${\;}_{8}^{16}$O | |
| C. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 属于同种原子 | |
| D. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 的核内中子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com