
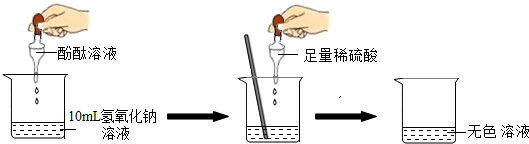
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
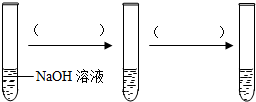
分析 (1)根据酚酞遇碱变红色分析,根据反应物、生成物写出化学方程式;
(2)根据生成的硫酸钠也与氯化钡反应生成硫酸钡沉淀和石蕊试液遇酸变红色以及活泼金属与酸反应生成氢气填写;
①氢氧化钠能与硫酸铜反应产生蓝色沉淀,能使酚酞变红色,使紫色石蕊试注解变蓝的性质分析如何判断氢氧化钠和稀硫酸反应发生.
解答 解:(1)酚酞遇碱变红色,所以氢氧化钠溶液使酚酞试液变红;氢氧化钠与稀硫酸反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;
故答案为:红;2NaOH+H2SO4=Na2SO4+2H2O;
(2)因为NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4,而石蕊试液遇酸变红色,所以方案二正确,因为活泼金属与酸反应生成氢气,所以可以加入锌粒等活泼金属(或碳酸钠等),若有气体放出,证明稀硫酸过量,反之稀硫酸不过量;故答案为:方案二;NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4;锌粒(或碳酸钠等);若有气体放出,证明稀硫酸过量,反之稀硫酸不过量;
①NaOH溶液和H2SO4溶液混合时没有明显的现象,氢氧化钠与硫酸铜反应生成蓝色沉淀,当氢氧化钠全被稀硫酸反应后,再加硫酸铜就不会产生蓝色沉淀,故可说明氢氧化钠与稀硫酸发生了反应,但加入的稀硫酸必须足量,故答案为:①足量H2SO4溶液 少量(或足量)CuSO4溶液;
(2)碱能使酚酞变红,酸不能使无色酚酞变色,故可用酚酞验证氢氧化钠和稀硫酸反应;紫色石蕊试液遇酸变红色遇到碱变蓝色,故也可用紫色石蕊检验氢氧化钠和稀硫酸反应,故答案为:酚酞试液(或石蕊试液).
点评 本题考查了酸碱中和反应,要完成此题可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的储备;对氢氧化钠与稀硫酸是否反应进行了探究,侧重基础又注重能力的培养,开放性问题有利于培养学生的发散思维并培养兴趣.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
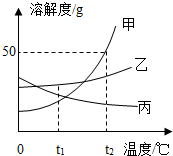 如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:
如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
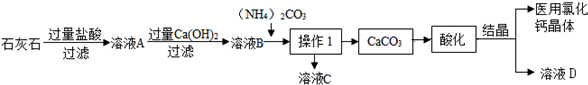
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
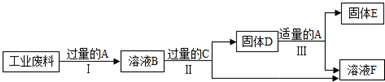
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
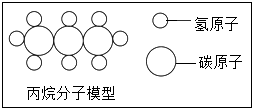
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
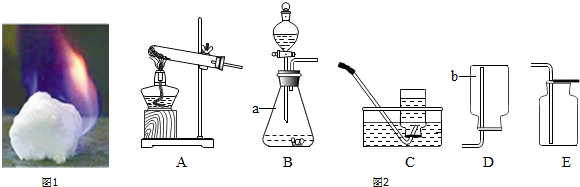
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
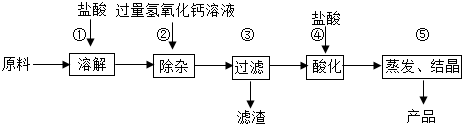
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com