
����Ŀ����ѧ��ȤС�����÷��ռ������Na2CO3��NaCl��MgCl2��CaCl2�ȣ���Na2CO3��10H2O��
����ȡ���̡�
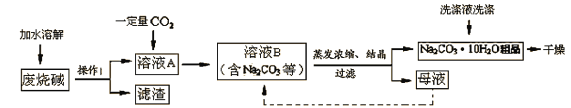
��������ϡ���Na2CO3+H2O+CO2��2NaHCO3
��2NaHCO3![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
����NaHCO3��Һ�м���BaCl2��Һ���ɷ�����Ӧ��2NaHCO3+BaCl2��BaCO3��+2NaCl+ H2O+CO2��
��̼���Ƶı�����Һ�ڲ�ͬ�¶��������ľ�������ͼ��ʾ��
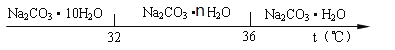
���������ۡ�
��1��������Ҫ�ɷ�ΪMg��OH��2�� ������Mg��OH��2�Ļ�ѧ����ʽ ��
��2����������ʹ�õIJ��������У��ձ��� �Ͳ�������
��3��ȡ������ҺB������BaCl2��Һ����ֻ�ϣ����۲쵽 ������������ҺB�к�NaHCO3��
��4���ᾧ����ʱ���¶������ �档
��5����ĸҺ������������������·��ѭ��ʹ�ã�ԭ���� ��ѡ����ţ���
�١�ĸҺ������Na2CO3
�ڡ�ĸҺ�����ѭ����NaCl��������
�����ȷ����
��6��ȡ�����ֲ�Ʒ����ˮ�ܽ⣬������ ��ѡ��������ţ���ͬ������ֽ��裬�ټ����� ��������֤�����в���NaCl��
��AgNO3��Һ ��ϡ���� ��ϡ����
��7����ȤС��ͬѧȡ32.8g����ֲ�Ʒ������ͼ��ʾװ�ã��г�����ʡ�ԣ�����ʵ�飺
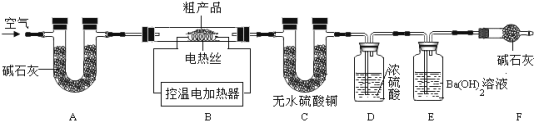
��������1��Na2CO3��10H2O������32������ʼ�ֽ�ʧˮ����ּ��ȿ���ȫʧˮ��NaHCO350��ʱ��ʼ�ֽ�270��ʱ��ȫ�ֽ⣻Na2CO3���Ȳ��ֽ⡣
��������2��Ba(OH)2��Һ������CO2��Ba(OH)2+CO2=BaCO3��+H2O
��ʵ��ǰҪ�� ����װ��ֲ�Ʒ��
װ��A�������� ��
���ֲ�Ʒ������270������ ����װ�ñ�ż�������֪�ֲ�Ʒ�к�NaHCO3�����C��D������m1��E��������m2����m1��m2 �����������=��������9��22��
ʵ����m2��1.1g���������32.8g�ֲ�Ʒ�к���NaHCO3������Ϊ g��
����������36��ʱ�����B��ʣ�����27.4g�����ʣ������� ���ѧʽ����NaHCO3�Ļ������˿�2�֣�
���𰸡���1��CaCO3�� 2Na OH+ MgCl2=2NaCl+Mg��OH��2��
��2��©��
��3����������
��4��32
��5����
��6���ۡ���
��7�������װ�õ������� ���տ����еĶ�����̼��ˮ����
��C�б�Ϊ��ɫ��E�в�����ɫ���� �� 4.2 ��Na 2CO3��7H2O
��������
������������������ۡ���1���ռ������������Ȼ�þ��Ӧ������������þ������̼�������Ȼ��Ʒ�Ӧ������̼��Ƴ�������������Ҫ�ɷ�Ϊ������þ��̼�������2������������Ҫ��������Һ����룬��Ϊ���˲���������Ҫ©������3���Ȼ�����̼�����Ʒ�����Ӧ���£�2NaHCO3+BaCl2��BaCO3��+2NaCl+ H2O+CO2�������������ݺͰ�ɫ����ʱ��֤����ҺB�к�̼�����ƣ���4���ᾧ����ʱ���¶������32��
��5����ĸҺ������������������·��ѭ��ʹ�ã�ԭ���ǡ�ĸҺ�����ѭ����NaCl������������ѡ��;�����ȷ�����ȼ����ᣬ��ȥ̼���ƣ�Ȼ�������������Һ�������Ȼ��ƣ����������Ȼ��Ʋ�����ɫ�������Ұ�ɫ�����Ȼ���������ϡ���ᡣ��ʵ��ǰҪ�ȼ��װ�õ������ԣ��ټ���ֲ�Ʒ����ʯ�������տ����е�ˮ�ֺͶ�����̼��������������ֲ�Ʒ������270��ʱ����ȫ�ֽ⣬����ˮ��������̼��̼���ƣ�������̼��ʹ����ʯ��ˮ����ǣ���ˮ����ͭ��ˮ��Ϊ��ɫ��̼���������ȷֽ����ˮ��̼���ƾ���ֽ�Ҳ�����ˮ��C��D������m1��������ˮ��������E��������m2��̼���������ȷֽ����������̼������2NaHCO3 ![]() Na2CO3+H2O+CO2�����м��㣬ˮ�Ͷ�����̼������Ϊ9��:22������m1��m2��9��22��
Na2CO3+H2O+CO2�����м��㣬ˮ�Ͷ�����̼������Ϊ9��:22������m1��m2��9��22��
�⣺��̼����������ΪX
2NaHCO3 ![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
168 44
X 1.1g
168/44=X/1.1g X=4.2g
����������36��ʱ,̼���������Ȳ���ֽ⣬��������̼����������Ϊ4.2g��֪���ֲ�Ʒ�к���̼�����ƾ���28.6g����̼��������=28.6g����106/136��100%��=10.6g����������36��ʱ�����B��ʣ�����27.4g��̼�����Ƶ�����Ϊ4.2g����̼���ƾ�������=27.4g-4.2g=23.2g ������ʽΪ��
23.2g ����106/106+18n��100%��=10.6g n=7����ѧʽΪ��Na 2CO3��7H2O


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������Ƚϣ���ѧϰ��ѧ����Ҫ����֮һ���Ա�CO��CO2�����ǵ����Ԫ�� �������ǵĻ�ѧ���� ����ҵ��CO������ұ������������������ �ԣ�
��2�����������õĿ���ʴ�ԣ����������ڿ�������������Ӧ�������������һ�����ܵ���������Ĥ���Ӷ���ֹ����һ������������������Ӧ�Ļ�ѧ����ʽΪ ��
��3������ɭ�֣�ע�����ͨ��״����ȼ����Ҫ�����������ٿ�ȼ�� ��������������� �� ����ɭ�ַ�������ʱ�����������·��ǰ��һƬ��ľ�������γɸ�����������ԭ���� ��
��4������Ʒ��ʴ�Ĺ��̣�ʵ��������������е�______�� �ȷ�����ѧ��Ӧ�Ĺ��̡�д����ֹ����Ʒ��ʴ��һ�ַ����� ��
��5��������ʯѡ�ó�������Ҫ�ɷ���������������ʾ����ԭ���Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᡢ���ᡢ���ᶼ�dz������ᣬ֮������Ϊ�������ᣬ����Ϊ
A�����Ƕ�����ζ
B�����ǵ�PHС��7
C��������ʹ���ָʾ����ɫ
D�����ǵ��������������ֻ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƫ���ᱵ��BaTiOx�����������ġ�ѹ��ЧӦ�����㷺Ӧ���ڳ���������װ���С���֪ƫ���ᱵ����Ԫ�صĻ��ϼ�Ϊ+4�ۣ����仯ѧʽ��x����ֵ��
A��1 B��2 C��3 D��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϴ��ܷ����õķ������ƽԭ������ԭʱ�����ϴ���������Ϊ���ڵ��������
A���������� B���������� C��������� D���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����7�֣�ijͬѧ��������þ��������з�̪��NaHCO3������Һ�У������������ݺͰ�ɫ���壬��Һ��ɫ���
һ����Һ��ɫ�����Ӧ����Һ�ļ��� �����ǿ���������䡱����������
����Ϊȷ���������ijɷ֣���ͬѧ���������µ�̽����
��1����ȼ���������壬���浭��ɫ����ȼ�ղ���ͨ�����ʯ��ˮ�У��������������Ϊ ��д��ѧʽ����
��2����ɫ�����������²²Ⲣ����ʵ�飺
���²⡿
��������1��Mg(HCO3)2������ˮ��
�� ��ɫ���������MgCO3��
�� ��ɫ��������� ��
�� ��ɫ���������MgCO3��Mg(OH)2��
��ʵ�顿
�� ȡϴ����İ�ɫ���壬���������� ��Һ���۲쵽 �����ɫ����һ������MgCO3��
��������2��MgCO3 ��Mg(OH)2�����ֽ⣬�ֱ��������������
��Ϊ��һ��ȷ����ɫ�������ɣ���ͬѧ�����˶���ʵ�飺
��ȡ����İ�ɫ����22.6 g����ּ��������ٲ�������Ϊֹ����ʹ�ֽ����������ȫ����ͨ��Ũ���ᣬŨ��������1.8g�����ɫ�����к��� ����ͨ����ʯ�ң���ʯ������8.8g���������MgCO3 ��Mg(OH)2��������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���;������������ء�����˵������ȷ��
A.ͭ�����Ƶ��ߣ�������ͭ�����õĵ�����
B.ϡ�����峣������������������ϡ������Ļ�ѧ���ʲ�����
C.�����������֣��������������п�ȼ��
D.����������ȡ���ʺ����ᣬ�������˵��������������ʷ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ȼ�գ��������䡢���ɺ�ɫ������ǣ� ��
A��ľ̿ B��þ�� C������ D����˿
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȱ��������״���״���ȱ��Ӱ���������������˼ά�ٶۣ����ͼ����Ϣ�жϣ�����������ȷ����
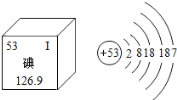
A����ԭ�ӵ�������126.9g
B�������ӣ�I�����ĺ��������Ϊ54
C����������������Ԫ�أ�����Խ��Խ��
D����ԭ�Ӻ�����5�����Ӳ㣬�μӻ�ѧ��Ӧʱ��ʧȥ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com