
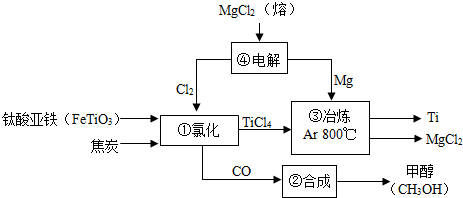
分析 (1)根据在化合物中正负化合价代数和为零,进行分析解答.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(3)③中反应,即镁与TiCl4在800℃,在氩气的环境中反应生成氯化镁和钛,写出反应的化学方程式即可.
(4)②中反应,即一氧化碳与氢气反应生成甲醇,写出反应的化学方程式,计算出理论上CO和H2投料的质量比即可.
(5)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
解答 解:(1)钛酸亚铁中铁元素显+2价,氧元素显-2价,设钛元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×3=0,则x=+4价.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,反应前铁、钛、氧、碳、氯原子个数分别为2、2、6、6、14,反应后的生成物中铁、钛、氧、碳、氯原子个数分别为0、2、6、6、8,根据反应前后原子种类、数目不变,则,2X分子中含有2个铁原子和6个铁原子,则每个X分子由1个铁原子和3个氯原子构成,则物质X的化学式为FeCl3.
(3)③中反应,即镁与TiCl4在800℃,在氩气的环境中反应生成氯化镁和钛,反应的化学方程式TiCl4+2Mg$\frac{\underline{\;\;\;\;\;Ar\;\;\;\;\;}}{800℃}$Ti+2MgCl2.
氩气的化学性质很不活泼,该反应在氩气(Ar)中进行的理由是防止Mg、Ti被氧化.
(4)②中反应,即一氧化碳与氢气反应生成甲醇,反应的化学方程式为CO+2H2═CH3OH.为使原料全部转化为甲醇,理论上CO和H2投料的质量比为28:(2×2)=7:1.
(5)既是反应物,也是生成物的物质,可以循环使用,以上流程中可用于循环的物质除Cl2、Mg外,还有MgCl2.
故答案为:(1)+4;(2)FeCl3;(3)TiCl4+2Mg$\frac{\underline{\;\;\;\;\;Ar\;\;\;\;\;}}{800℃}$Ti+2MgCl2;防止Mg、Ti被氧化;(4)7:1;(5)MgCl2.
点评 本题难度不大,理解冶炼金属钛和生产甲醇的工艺流程,掌握化合价的原则、质量守恒定律、化学方程式的书写方法等是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用小苏打焙制糕点 | B. | 油锅中的油着火用锅盖盖灭 | ||
| C. | 冬天用煤取暖时封闭门窗 | D. | 用过的菜刀用抹布擦干放置防生锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Na:“2”表示两个钠元素 | |
| B. | NO2:“2”表示一个二氧化氮分子含有两个氧原子 | |
| C. | $\stackrel{+2}{Mg}O$:“+2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | 2OH-:“2”表示两个氢氧根离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com