
| ||
| ||


科目:初中化学 来源: 题型:
| A、铁丝在氧气中燃烧火星四射 |
| B、镁条在空气中燃烧发出耀眼的白光 |
| C、红磷在空气中燃烧产生大量白烟 |
| D、铜片投入到稀硫酸中产生大量的气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 配料表 | 精制海盐,碘酸钾 |
| 含碘量/kg | 30mg~60mg |
| 包装日期 | 见封底 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、铝的金属活动性比铁强,说明铝制品比铁制品更容易锈蚀 |
| B、使用洗洁精清洗餐盘油污,运用了乳化的原理 |
| C、实验室一般使用大理石和稀硫酸制取二氧化碳 |
| D、质子数决定了元素的种类,说明质子数相同的微粒一定属于同一种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:
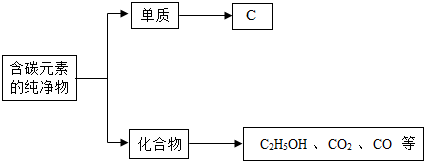
查看答案和解析>>
科目:初中化学 来源: 题型:
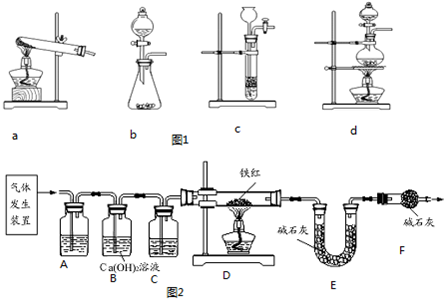
| 浓H2SO4 |
| △ |
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com