
根据金属的性质可知:铁和铜都能与氯化铁溶液反应,反应的化学方程式为:
Fe+2FeCl3 3FeCl2,
Cu+2FeCl3CuCl2 + 2FeCl2
3FeCl2,
Cu+2FeCl3CuCl2 + 2FeCl2
若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后烧杯中有金属剩余。下列分析正确的是
A.剩余金属只有Fe
B.剩余金属一定有Cu
C.反应后的溶液中可能有FeCl3
D.反应后的溶液中一定有FeCl2
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
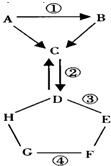 整理、归纳物质性质之间的相互联系,是化学学习的一 种有效方法.如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“--”表示两端的物质能发生化学反应).A、G都是单质,其中G是广泛应用的金属材料,元素G是人体必需的微量元素;气体C常用于灭火;F是一种蓝色溶液,可用于配制农药波尔多液.请你回答:
整理、归纳物质性质之间的相互联系,是化学学习的一 种有效方法.如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“--”表示两端的物质能发生化学反应).A、G都是单质,其中G是广泛应用的金属材料,元素G是人体必需的微量元素;气体C常用于灭火;F是一种蓝色溶液,可用于配制农药波尔多液.请你回答:查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省南京市建邺区中考一模化学试卷(解析版) 题型:推断题
下图中的物质为初中化学所学的物质,

其中甲、乙属于常见单质,其余均为化合物。且B为黑色固体,E为难溶性固体,A、C、D、E为不同类别的物质。
请回答:
(1)写出E的化学式 。
(2)G和H在组成上有何特点 。
(3)写出下列反应的化学方程式
A→B ;
F→E 。
【解析】B为黑色固体,根据常见的黑色固体,可以假设B为氧化铜,那么A应该为氢氧化铜,而甲为单质,且可以和单质乙互为生成物,并且能够和B反应,所以可以判断甲为氢气,而乙为活泼金属,例如铁,D可以生成甲,则可以判D为盐酸或是硫酸;A可以生成C,D通过反应也可以生成C,所以可以判断C为水,根据D为为酸,结合酸的性质及刚才的推断,可与判断E为盐类,由题意可知E为难溶性固体,所以可以判断E为碳酸钙,那么G为二氧化碳,进而判断F为碳酸钠,而H为一氧化碳,把各物质带入图框中验证,符合题意,可以据此答题.
查看答案和解析>>
科目:初中化学 来源: 题型:
根据金属的性质可知:铁和铜都能与氯化铁溶液反应,反应的化学方程式为:

 Fe+2FeCl3 3FeCl2, Cu+2FeCl3 CuCl2 + 2FeCl2
Fe+2FeCl3 3FeCl2, Cu+2FeCl3 CuCl2 + 2FeCl2
若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后烧杯中有金属剩余。下列分析正确的是 ( )
A.剩余金属只有Fe B.剩余金属一定有Cu
C.反应后的溶液中可能有FeCl3 D.反应后的溶液中一定有FeCl2
查看答案和解析>>
科目:初中化学 来源:2012届广东省佛山市高中阶段学校招生模拟考试(二)化学试卷(带解析) 题型:单选题
根据金属的性质可知:铁和铜都能与氯化铁溶液反应,反应的化学方程式为:
Fe+2FeCl3 3FeCl2,Cu+2FeCl3
3FeCl2,Cu+2FeCl3 CuCl2 +2FeCl2
CuCl2 +2FeCl2
若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后烧杯中有金属剩余。下列分析正确的是
| A.剩余金属只有Fe |
| B.剩余金属一定有Cu |
| C.反应后的溶液中可能有FeCl3 |
| D.反应后的溶液中一定有FeCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com