
某化学兴趣小组在老师指导下,进行了“H
2O
2生成O
2的快慢与什么因素有关”的实验.请你帮助回答下列问题.(实验均在20℃室温下进行)
(1)“用过氧化氢和二氧化锰制氧气”的反应方程式为:
.该操作过程中合理的排列顺序是:检验装置的气密性→将水槽中待收集气体的小试管注满水→
③
③
→
①
①
→
②
②
(选填序号).①待有连续稳定气泡再排水集气 ②旋紧连有导管的单孔胶塞
③向大试管内倒入适量过氧化氢再加入少许MnO
2粉末用试管进行排水法集气时,出现如图所示的3种操作,其中合理的是
C
C
.
若要证明MnO
2是该反应的催化剂,还需要增加实验来验证MnO
2在反应前后的化学性质和
质量
质量
是否改变.
(2)假设H
2O
2生成O
2的快慢与催化剂种类有关.在两瓶等体积6%的H
2O
2溶液中分别加入相同质量MnO
2和红砖粉,测量各生成一瓶(相同体积)O
2所需要的时间.记录数据如下:
| 实验编号 |
1 |
2 |
| 反应物 |
6% H2O2 |
6% H2O2 |
| 催化剂 |
1g红砖粉 |
1g MnO2 |
| 时间(s) |
152 |
35 |
由此得出的结论是
在相同条件下,H2O2生成O2的快慢与催化剂种类有关
在相同条件下,H2O2生成O2的快慢与催化剂种类有关
.
(3)假设H
2O
2生成O
2的快慢与不同质量分数的H
2O
2溶液有关.
在不同质量分数的H
2O
2溶液进行实验.记录数据如下:
| 实验编号 |
1 |
2 |
3 |
| H2O2溶液的溶质质量分数 |
5% |
10% |
20% |
| MnO2粉末用量(g) |
0.2 |
| 收集到500mL气体时所用时间(s) |
205 |
80 |
9 |
| 反应后溶液的温度(℃) |
39 |
56 |
67 |
从实验中得知该反应是个
放热
放热
反应(填“放热”或“吸热”),反应随H
2O
2溶液的质量分数的增加反应后液体温度逐渐
升高
升高
(填“升高”或“降低”).H
2O
2溶液的质量分数是怎样影响反应快慢?
在相同条件下,过氧化氢溶液中溶质的质量分数越大,反应速率越快
在相同条件下,过氧化氢溶液中溶质的质量分数越大,反应速率越快
.
(4)还有哪些因素可能影响该反应快慢?
请说出你的一个猜想:
其他条件不变时,改变此反应的温度,可影响此反应的速率
其他条件不变时,改变此反应的温度,可影响此反应的速率
.



 一课一练课时达标系列答案
一课一练课时达标系列答案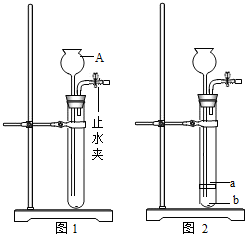 (2012?东营)实验室制取O2或CO2气体的发生装置如图1,请回答下列问题:
(2012?东营)实验室制取O2或CO2气体的发生装置如图1,请回答下列问题: (2004?锦州)某校化学研究性学习小组的同学在一次校外活动中看到铁匠师傅把红热的铁块浸入水中,产生“嗞嗞”声音,并有气泡产生,铁块表面生成一层黑色固体.铁匠师傅告诉他们,这叫做“淬火”.通过查找资料,得知“淬火”过程中铁与水发生3Fe+4H2O
(2004?锦州)某校化学研究性学习小组的同学在一次校外活动中看到铁匠师傅把红热的铁块浸入水中,产生“嗞嗞”声音,并有气泡产生,铁块表面生成一层黑色固体.铁匠师傅告诉他们,这叫做“淬火”.通过查找资料,得知“淬火”过程中铁与水发生3Fe+4H2O 某化学兴趣小组在老师指导下,进行了“H2O2生成O2的快慢与什么因素有关”的实验.请你帮助回答下列问题.(实验均在20℃室温下进行)
某化学兴趣小组在老师指导下,进行了“H2O2生成O2的快慢与什么因素有关”的实验.请你帮助回答下列问题.(实验均在20℃室温下进行)