某同学按照老师要求,配制20g 10%的氯化钠溶液,但是发现实验室没有纯净的氯化钠,只有含泥沙的粗盐.经过与同学的讨论,打算按如下步骤配制溶液:
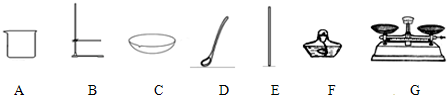
步骤一:粗盐提纯
(1)溶解:称取10g粗盐并加水溶解,需要用到上图中哪些仪器
AE
AE
.(填字母)
(2)过滤:在该操作中上图缺少的关键仪器是
漏斗
漏斗
.
(3)蒸发结晶:将滤液倒入蒸发皿中加热,当
出现较多晶体时
出现较多晶体时
可以停止连续加热.
(4)在上述三步操作中,均需要用到仪器E,其作用分别是
加速粗盐的溶解
加速粗盐的溶解
、
引流
引流
、
使液体受热均匀,防止外溅
使液体受热均匀,防止外溅
.
步骤二:配制溶液
(1)计算:需要氯化钠质量
2
2
克,需要水
18
18
mL.
(2)称量:用天平称取提纯后所得的精盐,并用
量筒
量筒
(填仪器名称)量取水.
(3)溶解:溶解时在烧杯中先加入
氯化钠
氯化钠
再加入
水
水
.充分溶解后得到的溶液中所含的微粒有
H2O、Na+、Cl-
H2O、Na+、Cl-
(填微粒符号).
(4)装瓶并贴上标签.
实验反思:
(1)若将20g 10%的氯化钠溶液稀释成5%的溶液,需加水
20
20
mL.
(2)该同学配制的溶液经测定溶质质量分数小于10%,下列哪些原因可能引起该误差
A
A
A.提纯后所得的粗盐不纯净,仍然含有可溶性的杂质
B.量取水视线与液体凹液面最低处相平
C.溶液配制好后装入试剂瓶时有部分洒到桌面上
D.称取固体时最终天平指针偏左.





