
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化锰(MnO2)粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间(t) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 |
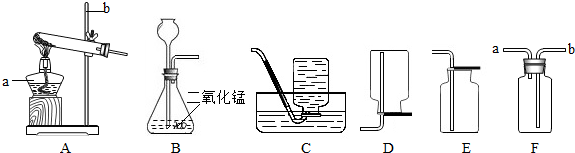
| 加热 |
| 加热 |
| 二氧化锰 |
| 二氧化锰 |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
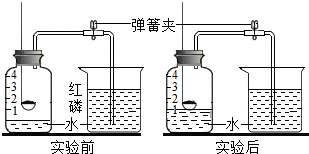 某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探究:
某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探究:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 观察到的现象 | 实验结论 |
| ①取少量固体配成溶液于试管中, 加入过量的CaCl2溶液. |
固体只有 部分变质 | |
| ②取少量充分反应后的溶液于试管中,滴入 |
溶液变红 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com