
【题目】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
(1)上述下图中,甲可表示________的溶解度曲线。
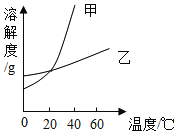
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是_____________。
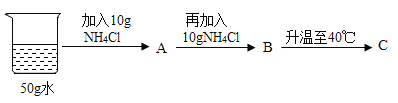
(3)20℃时,按下图所示操作:B中的溶液是________(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为_______。
【答案】KNO3或硝酸钾 NH4Cl或氯化铵 饱和 2:5
【解析】
(1)甲的溶解度随温度变化较大,比较硝酸钾和氯化铵在各个温度下的溶解度,可知0℃时,20℃时,硝酸钾溶解度都比氯化铵溶解度小,结合图像,甲可表示硝酸钾的溶解度曲线。
(2)饱和溶液的溶质质量分数为:![]() ,故比较饱和溶液的质量分数,比较该温度下的溶解度即可。60℃时,硝酸钾的溶解度大于氯化铵溶解度,故两种物质的饱和溶液中,溶质质量分数较小的是氯化铵。
,故比较饱和溶液的质量分数,比较该温度下的溶解度即可。60℃时,硝酸钾的溶解度大于氯化铵溶解度,故两种物质的饱和溶液中,溶质质量分数较小的是氯化铵。
(3)20℃时氯化铵的溶解度为37.2g,即该温度下100g水中最多溶解氯化铵37.2g,50g水中最多溶解18.6g,故A是不饱和溶液,B是饱和溶液,根据溶解度表,40℃时,50g水中最多溶解22.9g,故加入的20g溶质能全部溶解,则溶液的溶质和溶剂质量比为20:50=2:5。


科目:初中化学 来源: 题型:
【题目】碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用,我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界技术的发展。
(查阅资料)①生产原料粗盐中含有少量可溶性杂质(MgCl2 和 CaC12)及不溶性杂质。
②氨气极易溶于水,二氧化碳能溶于水。
③生产原理:NaCl + NH3 + CO2+ H2O = NaHCO3↓+ NH4C1,分离得晶体 A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是 NH4Cl===NH3↑+HCl↑。
⑤部分生产流程如下图所示:
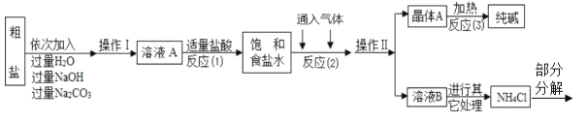
(问 题讨论)
(1)溶液 A 中的溶质为 ________,流程中加入适量盐酸的作用是 ________。
(2)反应(2)中为提高产率,所通入气体的顺序是 ________(填字母序号).
A.先通入 CO2 再通入 NH3 B.先通入 NH3 再通入 CO2
(3)上述生产流程中可循环使用的是 ________(填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(组成确定)
(1)称取一定质量的纯碱样品,多次充分加热,称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀 HNO3,再滴加 AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 ________(写化学式).
(含量测定) 同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下三组实验。甲组:取 12.0g 纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。将反应所得溶液小心蒸发,并将所得物质干燥、冷却至室温称得固体质量为 13.1g.样品中碳酸钠的质量分数为________。
乙组:取 12.0g 纯碱样品,利用下图所示装置,测出反应装置 C 增重了 4.1g(所加试剂均足量,每一步都反应完全).实验结束,发现乙组测定的质量分数偏小,其原因是_________。
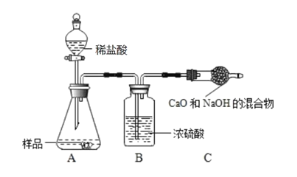
丙组:取 12.0g 的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀过滤、 洗涤、烘干称量固体质量,从而计算出碳酸钠的质量分数。组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是 ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食品营养与安全关系到每个人的身体健康。
(1)豆浆已成为众多家庭的早餐选择,下表是豆浆中部分成分的平均含量。
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素 |
平均含量(%) | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
豆浆的成分中能作为机体生长、修补受损组织的原料的是________,人体缺少表中的________元素会引起贫血。
(2)霉变的花生中含有黄曲霉毒素(化学式![]() )食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
)食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某市化学实验考查有:①氧化碳的制取;②配制50g5%的NaCl溶液;③实验室制取氧气……等六个考签,由学生抽签确定一个考题进行考查。
(1)甲同学抽签后来到实验室,发现本组实验桌上主要准备了下列仪器和药品:
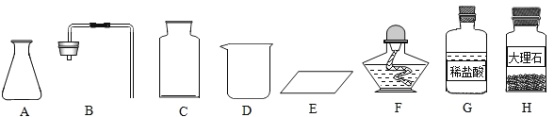
①甲同学抽到的考签应该是________________(填字母代号)。
A氧气的制取 B二氧化碳的制取
②制取该气体的反应原理为________________________(用化学方程式表示)。制取一瓶该气体,应选用的仪器有___________________(填字母代号)。
(2)乙同学在完成“配制50g5%的NaCl液”实验过程中,通过计算,他需量取的水的体积约为_____________mL 。溶解NaCl时用到的玻璃棒的作用是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)“健康饮食、均衡营养”是青少年健康成长的重要保证。
①蛋白质是构成细胞的基本物质,是机体生长和修补受损组织的主要原料。处于生长发育期的青少年每天需要较多的蛋白质。下列物质中富含蛋白质的有______(填字母)。
A 米饭和馒头 B
米饭和馒头 B 大豆油和花生
大豆油和花生
C 瘦肉和鸡蛋 D
瘦肉和鸡蛋 D 蔬菜和水果
蔬菜和水果
②“食品安全”是一个永恒的话题。你认为下列认识不科学的是_________(填字母)。
A 加工制作食品时可以严格按照国家规定使用食品添加剂
B 霉变的大米、花生,即使经过蒸煮也不能食用
C 含钙、锌的奶粉有利于补充人体所需的常量和微量元素
D 用亚硝酸钠代替食盐来腌渍食品
(2)科技发展促进了新材料的生长和使用,也极大地促进了人类社会的发展与进步。
①目前,“辽宁号”航母已形成战斗力,第一艘国产航母即将下水海试。特种钢铁是制造航母甲板的主要材料,它易与空气中的_________等物质发生反应而锈蚀,请你列举一种防止钢铁锈蚀的方法___________________。
②英国向“一次性塑料文化”开战。2018年4月19日宣布,将全面禁用一次性塑料袋、棉签、吸管和搅拌棒等塑料制品,以保护环境。塑料属于__________材料(填“复合”或“有机合成”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。
(1)在石墨、干冰、硫酸铜三种物质中,由分子构成的物质是___________(填化学式)。
(2)根据如图的信息回答问题:
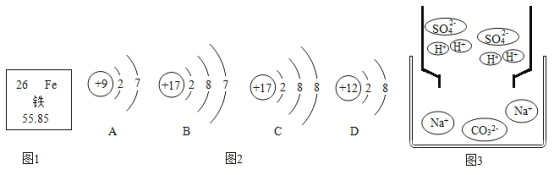
①图1中铁元素的相对原子质量是__________;铁原子失去3个电子形成离子的名称为__________。
②图2中,A、B粒子化学性质相似的主要原因是___________;D 元素位于周期表第___________周期。
C、D两种元素形成化合物的化学式__________。
(3)图3是碳酸钠溶液和稀硫酸反应的微观示意图该反应的微观实质是____________,反应后所得溶液中的溶质是___________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列方案设计不能达到实验目的的是( )
选项 | 物质 | 目的 | 主要实验操作 |
A |
| 除杂 | 先通过 |
B |
| 分离 | 溶解、过滤、洗涤、干燥、蒸发 |
C |
| 检验是否变质 | 取样,滴加足量稀盐酸,观察现象 |
D |
| 比较活动性 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一固体混合物A,其中可能含![]() 三种物质中的两种或多种,还有一固体混合物B,其中可能含
三种物质中的两种或多种,还有一固体混合物B,其中可能含![]() 三种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。
三种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。
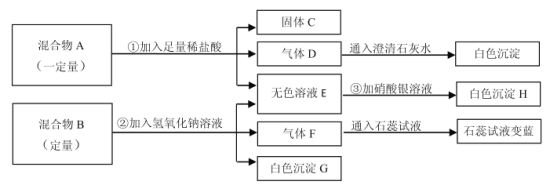
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)生成的气体F的气味为____________。
(2)白色沉淀G的化学式为___________,白色沉淀H的名称为____________。
(3)溶液E中肯定大量存在的酸根阴离子是___________。
(4)在混合物A中,一定存在的物质是_____________。
(5)写出过程①中发生反应的化学方程式为_______________。
(6)在混合物B中肯定不存在的物质是(写化学式)______,请简述理由是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用红磷燃烧的方法测定空气中氧气的含量:

(1)在集气瓶中加入少量水,并将水面上方空间分成5等份,如图装置所示。待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此可知氧气约占空气总体积的____________。
(2)实验后发现测定空气中氧气含量偏低,造成这种结果的可能原因是(填一种即可):______。
(3)这个实验还可以推测出氮气的性质为____________。
(4)写出红磷在空气中燃烧的文字表达式______。
(5)已知:镁+氧气![]() 氧化镁,氮气+镁
氧化镁,氮气+镁![]() 氮化镁(固体),根据上述反应,能否用镁代替磷测定空气的成分?为什么___________?
氮化镁(固体),根据上述反应,能否用镁代替磷测定空气的成分?为什么___________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com