
分析 反应中只有二氧化锰是固体物质,所以“洗涤、干燥后得滤渣”即为二氧化锰;又二氧化锰在反应中是催化剂,反应前后质量不变,所以反应前各物质的质量总和应为过氧化氢溶液和二氧化锰的质量和.反应中仅有氧气放出,再利用质量守恒定律即可求得氧气的量.最后利用所求氧气的质量求出过氧化氢溶液中溶质过氧化氢的质量.
解答 解:生成氧气质量为:50g+3g-51.4g=1.6g
设50g双氧水溶液中H2O2的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}=\frac{32}{1.6g}$
x=3.4g
答:所得溶液溶质质量为3.4g.
点评 本题为最基本的根据化学方程式的计算题,解答本题的关键是根据质量守恒定律求出氧气的质量.


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | K+、OH-、NO3- | B. | K+、Na+、SO42- | C. | Ca2+.CO32-、Cl- | D. | NH4+、Cu2+、Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是小明利用红磷燃烧来探究空气中氧气的含量,试分析:
如图是小明利用红磷燃烧来探究空气中氧气的含量,试分析:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
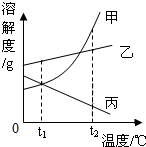 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | t1℃时,甲、乙、丙三种物质的溶解度大小关系是:乙>甲>丙 | |
| B. | 分别加入溶质或降低温度都可使t2℃时甲、乙、丙的不饱和溶液变为饱和溶液 | |
| C. | 将甲、乙两种物质的饱和溶液温度由t2℃降到t1℃时,甲析出的晶体质量一定比乙多 | |
| D. | 将甲、乙、丙的饱和溶液温度由t2℃降到t1℃时,所得溶液中溶质质量分数由大到小的顺序为:乙>甲>丙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应:
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应:| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com