
图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.请你回答:
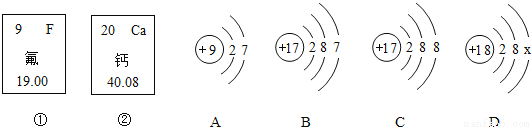
(1)钙元素的相对原子质量为_____,氟元素的原子序数为_____,D中的X为_____,氯原子的符号是_____,钙离子的符号为_____;
(2)①②中不同种元素最本质的区别是_____;
(3)A、B、C、D结构示意图中,属于同种元素的粒子是_____(填字母);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_____(填字母).
40.08 9 8 Cl Ca2+ 质子数不同 BC B 【解析】(1)由图可知,钙元素的相对原子质量为40.08;氟元素的原子序数为9;由核内质子数=核外电子数得,D中的X为8;原子符号直接用元素符号来表示,故氯原子的符号是Cl;钙元素的原子结构示意图中最外层的电子数是2,易失去2个电子,故化合物中显+2价,故钙离子的符号为Ca2+; (2)①②中元素的质子数不同,故种类不同; ...科目:初中化学 来源:陕西省西安市2018届九年级中考化学一模化学试卷 题型:简答题
溶解是生活中常见的现象,不同物质在水中的溶解能力不同。
用硫酸铜进行如图所示的实验,观察后完成下列填空(用编号表示)
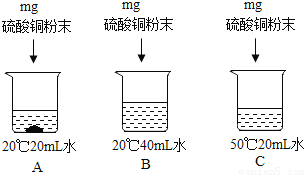
(1)硫酸铜的溶解度随温度升高_____(填“变大”或“不变”或“变小”)。
(2)所得三个溶液中:一定属于饱和溶液的是_____,溶液中溶质质量的大小关系是_____。
变大 A B=C>A 【解析】本题考查了固体溶解度的影响因素,饱和溶液和不饱和溶液判定。 (1)由图示知,硫酸铜的溶解度随温度升高而变大; (2)通过分析可知,A烧杯底部有固体,所以一定属于饱和溶液的是A,A中的溶质有剩余,B、C中的溶质分别为mg,所以溶液中溶质质量的大小关系是:B=C>A。查看答案和解析>>
科目:初中化学 来源:哈尔滨市升学考试模拟调研测试(一)化学试卷 题型:单选题
对下列事实解释错误的是( )
选项 | 事 实 | 解 释 |
A | 氧气加压可变成液氧 | 加压可使分子体积变小 |
B | 金刚石很硬,石墨质软 | 碳原子排列方式不同 |
C | 过氧化氢溶液是混合物 | 由不同种分子构成 |
D | 宝石绚丽多彩 | 宝石中含有某些金属离子 |
A. A B. B C. C D. D
A 【解析】A、氧气加压后变成液氧,分子的体积没变,分子之间的间隙变大,错误; B、由于金刚石和石墨的碳原子排列方式不同,故物理性质不同,正确; C、过氧化氢溶液是由不同的分子构成,故是混合物,正确; D、宝石中含有某些金属离子,故宝石中含有某些金属离子,正确。故选A。查看答案和解析>>
科目:初中化学 来源:北京市2018届九年级中考化学专题复习:金属与氧气和酸的反应 题型:单选题
一废旧家用电器的某部件含有Zn、Fe、Cu三种金属,若与足量稀盐酸充分反应,过滤后剩余的金属是
A. Zn、Fe B. Zn C. Fe D. Cu
D 【解析】试题分析:Zn、Fe、Cu三种金属的活动性为Zn>Fe>H>Cu;若与足量稀盐酸充分反应,Zn与Fe反应,Cu不参加反应,故选D查看答案和解析>>
科目:初中化学 来源:贵州省遵义市2018届九年级上学期期末化学试卷 题型:计算题
“黄铜”是铜锌合金,具有较强机械性能,街头许多“金色”饰品就是用它来制作的.某研究性学习小组为了测定黄铜中铜的质量分数,称取20g黄铜样品,放入烧杯中,然后加入某浓度的稀盐酸100 g(足量),用玻璃棒搅拌至不再产生气泡为止(反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑),称量剩余物质的总质量为119.8g.请计算:
(1)实验过程中,产生氢气的质量_____,你的计算依据是_____.
(2)该铜锌合金中铜的质量分数为____________.
0.2g 质量守恒定律 67.5% 【解析】(1)实验中产生的氢气的质量为120g-119.8g=0.2g;计算依据是质量守恒定律; (2)设该合金中锌的质量为x Zn+2HCl═ZnCl2+H2↑ 65 2 x 0.2g =,求得x=6.5g 故合金中铜的质量为20g-6.5g=13.5g 样品中铜的质量分数为=67.5% 答:生成氢气的质量...查看答案和解析>>
科目:初中化学 来源:贵州省遵义市2018届九年级上学期期末化学试卷 题型:单选题
对于Fe、Fe2+、Fe3+三种微粒子判断,正确的是( )
①核电荷数相同 ②核外电子数相等 ③电子层结构完全相同 ④质量几乎相等 ⑤等质量的三种微粒所含的质子数相等.
A. ①④⑤ B. ①③⑤ C. ①④ D. ①②③④
A 【解析】Fe、Fe2+、Fe3+是铁元素的三种不同微粒,故核电荷数相同,Fe原子的最外层电子失去后形成了Fe2+、Fe3+,故核外电子数不相等,电子层结构也不同,原子的质量主要集中在原子核上,外出的电子可以忽略不计,故质量几乎相等,等质量的三种微粒所含的质子数相等.故①④⑤正确,选A。查看答案和解析>>
科目:初中化学 来源:江苏省2018届九年级上学期期末化学试卷 题型:科学探究题
铁和铁的化合物在工农业生产中有广泛的应用。
(一)铁的应用和防护
A.我国在西汉时期就有“曾青得铁则为铜”之说,用化学方程式表示其原理:_____。
B.铁生锈的主要过程为:
Fe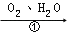 Fe(OH)2
Fe(OH)2 Fe(OH)3
Fe(OH)3 Fe2O3•xH2O
Fe2O3•xH2O
(1)写出转化①的化学方程式_____。
(2)转化③生成 Fe2O3•xH2O,则 x≤_____(x 为整数)。
C.请提出防止铁生锈的一条措施_____。
(二)铁的化合物应用
黄铁矿(主要成分是FeS2),是一种重要的化工原料,可用来制备硫酸和炼铁(图1)。

A.工业上将黄铁矿粉碎的目的是_____。
B.生产硫酸后的尾气中含有 SO2,如直接排放可能会造成环境问题是_____。
C.高炉炼铁的化学方程式为_____。
D.150 吨含 FeS280%的黄铁矿理论上最多可制得 98%的浓硫酸_____吨。
(三)铁的冶炼和探究
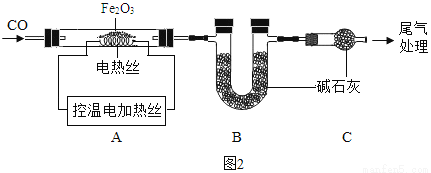
取 24.0g Fe2O3 粉末,小组同学用图2装置模拟炼铁,并测得反应后固体成分。
资料:碱石灰可吸收 H2O 和 CO2。
A.连接装置,先_____,再装入药品。
B.实验时先通入CO,目的是_____。
C.控制A中温度在 700℃至固体全部变黑,继续通CO至冷却。
(1)通过测定装置 B 中固体的质量变化,可准确求得装置 A 中剩余固体质量。装置C的作用是_____。
(2)现直接测得装置 A 中剩余固体质量为19.2g。则装置 B 中固体应增重_____g。
D.经分析A中剩余固体 19.2g 为Fe和 FexOy 的混合物,向其中加入足量的稀 H2SO4充分 反应,得 H20.3g。
(1)固体中 Fe 的质量为_____g。
(2)FexOy 的化学式为_____。
查看答案和解析>>
科目:初中化学 来源:江苏省2018届九年级上学期期末化学试卷 题型:单选题
下列物质在给定条件下的转化均能一步实现的是( )
A. Fe3O4  Fe
Fe FeCl3
FeCl3
B. H2O2  H2
H2  H2O
H2O
C. CaCl2溶液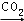 CaCO3
CaCO3  CO2
CO2
D. CuSO4溶液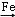 Cu
Cu 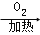 CuO
CuO
查看答案和解析>>
科目:初中化学 来源:江苏省泰州市姜堰区2018届九年级中考适应性(一模)考试化学试卷 题型:单选题
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是

A. P点表示t1℃时,a、c两溶液的溶质质量分数相等
B. 将c物质的饱和溶液变为不饱和溶液,可采用升温的方法
C. t2℃时,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液
D. 将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
C 【解析】A、t1℃时,a、c两种物质的溶解度都是20g,溶液是否饱和不确定,无法判断溶质的质量分数,错误;B、c的溶解度随温度的降低而升高,将c物质的饱和溶液变为不饱和溶液,可采用降温的方法,错误;C. t2℃时,a的溶解度是50g,t2℃时,100g水中最多溶解50g的a,50g的水最多溶解25g的a,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液,正确;D、将t1...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com