
【题目】酸、碱、盐是我们身边重要的化合物,在生活和生产中具有广泛的应用。
(1)某锅炉水垢的主要成分有CaCO3、Mg(OH)2、Fe2O3,用“酸洗”法可除去该水垢。但“酸洗”时,一般不选用稀硫酸的原因是_______________。
(2)春秋末期齐国的工艺官书《考工记》中载有“涑帛”的方法,即利用“灰”(草木灰:K2CO3)和“蜃”(贝壳灰:CaO)混合加水所得溶液来洗涤帛,这种溶液能洗涤丝帛是因为其中一定含有的物质是______________(水除外)。
(3)两种抗胃酸药剂的主要成分及建议每次剂量见下表:
主要成分 | NaHCO3 | Mg(OH)2 |
建议每次剂量/g | 0.5 | 0.3 |
①服用Mg(OH)2的药效比服用NaHCO3“强”的原因是_______________。
②写出NaHCO3与胃酸主要成分反应的化学方程式:________________。
【答案】硫酸与碳酸钙反应生成CaSO4微溶于水,覆盖在水垢表面,难以除尽 KOH ①等质量的Mg(OH)2消耗的盐酸比NaHCO3多 NaHCO3+HCl=NaCl+H2O+CO2↑
【解析】
(1)水垢的主要成分有CaCO3与硫酸反应生成硫酸钙,硫酸钙是微溶于水,覆盖在水垢表面,阻碍反应,难以除尽水垢。
(2)氧化钙和水反应生成氢氧化钙,氢氧化钙再与碳酸钾反应生成碳酸钙沉淀和氢氧化钾,其中氢氧化钾溶液呈碱性,性质与氢氧化钠相似,可以用于作洗涤剂。
(3)①Mg(OH)2与胃酸反应的化学方程式为![]() ,根据该方程式可算出参加反应的氢氧化镁和盐酸的质量比为58:73;NaHCO3与胃酸反应的方程式为
,根据该方程式可算出参加反应的氢氧化镁和盐酸的质量比为58:73;NaHCO3与胃酸反应的方程式为![]() ,根据该方程式可算出参加反应的碳酸氢钠和盐酸的质量比为84:36.5=168:73;从它们的质量比可知,消耗相同质量的盐酸,碳酸氢钠用量大,氢氧化镁用量少,故服用Mg(OH)2的药效比服用NaHCO3“强”。
,根据该方程式可算出参加反应的碳酸氢钠和盐酸的质量比为84:36.5=168:73;从它们的质量比可知,消耗相同质量的盐酸,碳酸氢钠用量大,氢氧化镁用量少,故服用Mg(OH)2的药效比服用NaHCO3“强”。
②胃酸主要成分为盐酸,与NaHCO3反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑。


科目:初中化学 来源: 题型:
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
(1)电解水实验揭示了水的组成。下图实验中得到氧气的试管是_______(填“1”或“2”)。 (2)电解水的化学方程式为_________。
| (1)潜水时需要氧气,说明氧气能________。 (2)用高锰酸钾制取氧气的化学方程式为_________。
|
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸乙烯酯(C3H4O3)可用作锂电池电解液,下列有关碳酸乙烯酯的说法正确的是
A. 碳酸乙烯酯的相对分子质量为(12×3+1×4+16×3)g
B. 碳酸乙烯酯中C、H、O三种元素的质量比为12:1:16
C. 碳酸乙烯酯中C、H、O三种原子的个数比为3:4:3
D. 碳酸乙烯酯中碳元素的质量分数= ![]() ×100%
×100%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝及其化合物有极其重要的用途。
(一)铝的广泛应用
(1)铝是很活泼的金属,但用铝制做的炊具却耐腐蚀,其原因是____________(用方程式表示)。
(2)使用铝制炊具会使人体摄入过量的“铝”,导致记忆力减退等不良症状。这里的“铝”是指______________。
A单质 B元素 C原子 D分子
(二)硫酸铝铵晶体(NH4Al(SO4)2·xH2O)是一种用途广泛的含铝化合物。兴趣小组在科研人员指导下,设计实验探究硫酸铝铵晶体受热分解的产物。
(查阅资料)①SO2可与稀KMnO4溶液反应使其褪色。
②SO3+H2O=H2SO4。
③硫酸铝铵热分解完全可得到纳米氧化铝。
④碱石灰是CaO和NaOH的混合物。
(1)硫酸铝铵(NH4Al(SO4)2)中铝元素的化合价为____________。
(2)硫酸铝铵晶体分解产物的定性探究
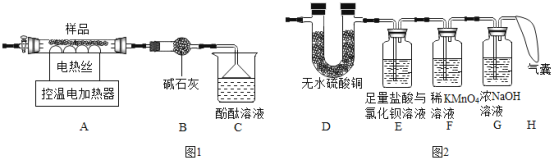
①装置C中观察到酚酞溶液变红色,由此可知分解的产物中有__________(写化学式)。
②某同学认为硫酸铝铵晶体受热分解的产物中还有H2O、SO2、SO3和N2。为进行验证,用图1中的装置A和图2所示装置连接进行实验。实验中,装置D中现象是___________________ ,证明有H2O生成;装置E中现象是______________,证明有SO3生成;而装置F中现象是____________、H最终没有胀大,证明没有SO2和N2生成。
(三)硫酸铝铵晶体成分及分解产物的定量探究:为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如下图所示。
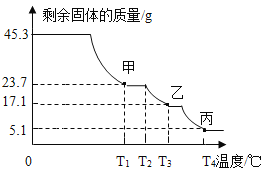
(1)固体甲是T1℃刚好完全失去结晶水的产物,则x =_________。(写出计算过程)
(2)T3℃时固体乙的成分是_______________(填字母)。
AAl2(SO4)3 BAl(OH)3 CAl2(SO4)3和Al(OH)3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应能一步实现,部分反应物、生成物和反应条件均已略去),请回答下列问题。
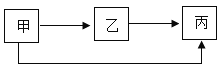
(1)若甲为黑色固体,甲、乙、丙的相对分子质量依次增大,且乙与丙是组成元素相同的两种气体,则丙的化学式为__________;乙→丙的反应类型__________(填“一定”或“不一定”)是化合反应。
(2)若丙为助燃性气体,甲与乙是组成元素相同的两种物质,则乙的化学式为_________,甲→丙反应的化学方程式为_______________。
(3)若甲、乙、丙均为碱,且丙为蓝色沉淀,写出甲→乙反应的化学方程式为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】揭开物质构成的奥秘,有利于研究物质的组成、构成和物质发生变化的实质,请回答下列问题。
(1)如图A是钠元素在周期表中的相关信息,B、C分别是氟(F) 原子、镁原子结构示意图。
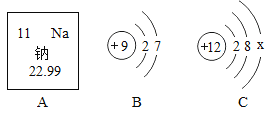
①钠原子的相对原子质量为_________;
②写出由镁元素和氟元素组成化合物氟化镁的化学式__________。
(2)下图是某化学反应的微观模拟示意图。
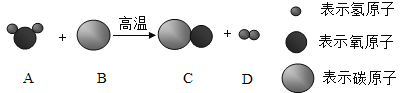
①该反应属于_______________(填基本反应类型)反应;
②化学变化前后,没有发生变化的粒子是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c 三种物质的溶解度曲线如下图所示。取等质量![]() ℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至
℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至![]() ℃。下列说法不正确的是
℃。下列说法不正确的是
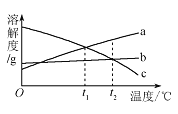
A. 原饱和溶液中,溶质的质量分数 a>b="c"
B. 恢复至 t2℃时,析出溶质的质量 a>b=c
C. 恢复至t2℃时,三种溶液一定都是饱和溶液
D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室化学实验装置,回答有关问题。

(1)请写出仪器的名称:a_____;b_____。
(2)实验室用氯酸钾制取氧气的反应方程式是_____;可用_____法收集氧气。制得的氧气用来![]() 、H的实验,发现H中铁丝不燃烧,其原因是_____。
、H的实验,发现H中铁丝不燃烧,其原因是_____。
(3)实验室若用装置E收集二氧化碳,则气体应从_____端进入(填“①”或“②“);若要获得干燥的二氧化碳,可将装置B和装置D用胶皮管连接,并在装置D中盛放_____(填试剂名称)。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是_____;下列可用C装置制备气体的是_____(填字母)。
a.双氧水和二氧化锰粉末制氧气
b.块状大理石和稀硫酸制二氧化碳
c.锌片和稀盐酸制氢气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铟是制造触屏的重要材料,相关信息如图,下列说法中正确的是
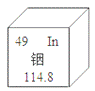
A.铟是一种非金属元素B.相对原子质量是114.8g
C.原子的核电荷数为49D.与其他元素根本区别是中子数不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com