
 ”“
”“ ”代表氢气分子和氮气分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请从微观角度回答下列问题:
”代表氢气分子和氮气分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请从微观角度回答下列问题: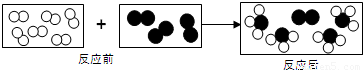
科目:初中化学 来源: 题型:阅读理解
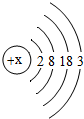 阅读材料,回答问题:
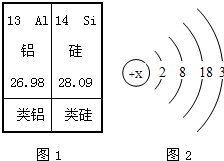
阅读材料,回答问题:| 13 Al 铝 26.98 |
14 Si 硅 28.09 |
| 类铝 | 类硅 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 ”“
”“ ”代表氢气分子和氮气分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请从微观角度回答下列问题:
”代表氢气分子和氮气分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如图所示,请从微观角度回答下列问题: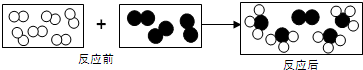
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 阅读材料,回答问题:
阅读材料,回答问题:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com