
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量Na2CO3溶液于试管中,加入少量的 酚酞试液 | 酚酞试液变红色 | Na2CO3水溶液呈碱性 |
| 实验编号 | Na2CO3溶液的溶质质量分数(均取2mL) | 实验温度 | pH |
| a | 1% | 20℃ | 11.6 |
| b | 1% | 30℃ | 11.8 |
| c | 5% | 20℃ | 12.1 |
| d | 5% | 30℃ | 12.4 |
分析 (1)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳密度比空气大,不能燃烧,不支持燃烧;
(2)碳酸钠溶液显碱性,能使酚酞试液变红色;
通过对比试验可以判断影响Na2CO3溶液酸碱度的因素;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠.
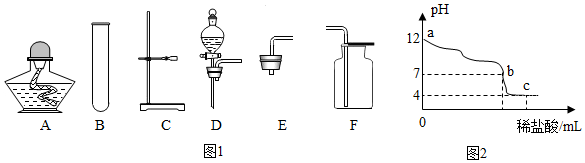
解答 解:(1)①用高锰酸钾制取氧气的发生装置可选择如图中的酒精灯A、试管B、铁架台C和带导管的单孔橡皮塞E.
故填:ABCE.
②实验室制取二氧化碳的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
用F收集二氧化碳时,通入二氧化碳一段时间后,接下来的操作是把燃烧的木条放在集气瓶口,木条熄灭,说明二氧化碳已经收集满,再移出导气管,盖上玻璃片.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;把燃烧的木条放在集气瓶口,木条熄灭.
(2)①取少量Na2CO3溶液于试管中,加入少量的酚酞试液,酚酞试液变红色,说明碳酸钠溶液显碱性,实验过程如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量Na2CO3溶液于试管中,加入少量的酚酞试液 | 酚酞试液变红色 | Na2CO3水溶液呈碱性 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题
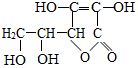 黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).
黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 检验食盐中是否含有氯元素 | B. | 检验自来水是否用氯气消毒 | ||
| C. | 检验鸡蛋壳是否可溶于酸 | D. | 确定味精的元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 步骤①可省略 | |
| B. | 滤液Ⅲ中有三种溶质 | |
| C. | 滤渣乙的物质的量等于原固体混合物中氯化钾的物质的量 | |
| D. | 滤渣乙和滤渣戊的物质的量之和等于②中加入的硝酸银的物质的量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
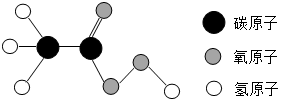 年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )
年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )| A. | 过氧乙酸分子的化学式为 C2H4O3,其相对分子质量为 76 | |
| B. | 过氧乙酸是一种化合物 | |
| C. | C、H、O三种元素的质量比为 2:4:3 | |
| D. | 完全燃烧可能会生成 CO2 和 H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 8 | 6 |
| 反应后质量/g | 4 | 待测 | 28 | 2 |
| A. | “待测”数值一定为2g | B. | 乙一定是该反应的催化剂 | ||
| C. | 反应中甲和丙的质量比为1:7 | D. | 该反应中甲、丁都是反应物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com