
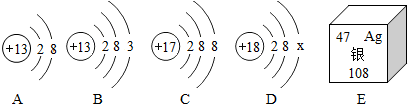
分析 (1)依据质子数不同元素种类不同分析解答;
(2)依据阳离子是质子数大于核外电子数,而阴离子是核外电子数大于核内质子数的特点分析解答;
(3)依据原子中质子数与核外电子数的关系分析解答;
(4)根据元素周期表中各部分的意义分析解答;
解答 解:(1)依据质子数不同元素种类不同,由图示可知四种微粒中共有质子数是13、17和18的三种元素;
(2)阳离子是质子数大于核外电子数,故A是带有三个正电荷的铝离子,符号为:Al3+;
(3)由于原子中质子数与核外电子数相等,观察可知该微粒的质子数是18,是具有稳定结构的氩原子,所以核外电子数也应为18,所以X为8;
(4)根据元素周期表中各部分的意义可知E中银元素原子的质子数为47.
故答案为:(1)三;(2)Al3+;(3)8;(4)47.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图和元素周期表的意义是正确解题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向一定量二氧化锰固体中加入过氧化氢溶液 | |
| B. | 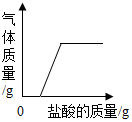 向一定量纯碱和烧碱的混合溶液中滴入盐酸 | |
| C. |  一定温度时向一定量饱和石灰水中加入氧化钙 | |
| D. |  向一定量稀硫酸中滴入水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合理施用农药、化肥,以减少水体污染 | |
| B. | 天然水中硬水属于混合物,软水属于纯净物 | |
| C. | 加强工业废水的排放监控,坚持达标排放 | |
| D. | 天然淡水经过沉降、过滤、杀菌消毒等净化过程变成自来水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com