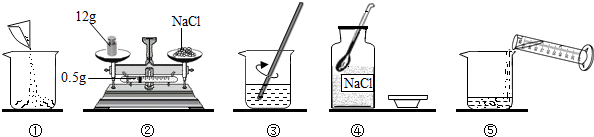
£Ø2013?Ī«·»£©Ä³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖ²ā¶Ø“æ¼īѳʷ£Øŗ¬NaClŌÓÖŹ£©ÖŠĢ¼ĖįÄĘÖŹĮæ·ÖŹżµÄŹµŃé·½°ø£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ģ¼ĖįøłĄė×Ó³Įµķ·Ø£®ŹµŃé²½Öč£ŗ
¢ŁÓĆĶŠÅĢĢģĘ½³ĘȔѳʷ·ÅČėÉÕ±ÖŠ¼ÓĖ®Čܽā£»
¢Ś¼ÓČė×ćĮæBaCl
2ČÜŅŗ³ä·Ö·“Ó¦£®Ö¤Ć÷·“Ó¦ŗóBaCl
2Ź£ÓąµÄ·½·ØŹĒ
¾²ÖĆ£¬Č”ÉŁĮæÉĻ²ćĒåŅŗµĪ¼ÓĢ¼ĖįÄĘČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬Ö¤Ć÷ĀČ»Æ±µŹ£Óą
¾²ÖĆ£¬Č”ÉŁĮæÉĻ²ćĒåŅŗµĪ¼ÓĢ¼ĖįÄĘČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬Ö¤Ć÷ĀČ»Æ±µŹ£Óą
£»
¢Ū¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘĮæ³ĮµķµÄÖŹĮæĪŖmg£»
¢Üѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹżĪŖ
£®
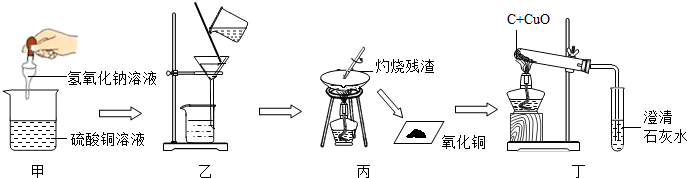
£Ø2£©ĘųĢå·Ø£®Ń§Ļ°Š”×éĄūÓĆČēĶ¼×°ÖĆ²ā¶Øѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹż£®
¢ŁŹµŃé×°ÖĆŅŅÖŠŹ¢·ÅµÄŹŌ¼ĮĪŖ
ÅØĮņĖį
ÅØĮņĖį
£¬×°Öƶ”µÄ×÷ÓĆŹĒ
·ĄÖ¹æÕĘųÖŠµÄ¶žŃõ»ÆĢ¼ŗĶĖ®ÕōĘų½ųČė±ūÖŠ
·ĄÖ¹æÕĘųÖŠµÄ¶žŃõ»ÆĢ¼ŗĶĖ®ÕōĘų½ųČė±ūÖŠ
£®
¢ŚŃ§Ļ°Š”×éĶعż²āĮæ±ū×°ÖĆŹµŃéĒ°ŗóµÄÖŹĮæ£®Č·¶Ø¶žŃõ»ÆĢ¼µÄÖŹĮ森ŹµŃéÖŠµĪ¼ÓĻ”ĮņĖįµÄĖŁ¶Č¹żæģ£¬²śÉśµÄĘųĮ÷¹ż¼±£®»įµ¼ÖĀ²āµĆѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹż
Ę«µĶ
Ę«µĶ
£ØĢīŠ“”°Ę«øß”±”°Ę«µĶ”±»ņ”°²»±ä”±£©£®
£Ø3£©²āĀČ»ÆÄĘ·Ø£®ĒėÄćĶź³ÉĻĀĮŠŹµŃé·½°ø£ŗ
³ĘČ”Ņ»¶ØÖŹĮæµÄѳʷ·ÅČėÉÕ±ÖŠ¼ÓĖ®Čܽā£ŗ
¼ÓČė×ćĮæĻ”ĻõĖį£¬ŌŁ¼ÓČė×ćĮæµÄĻõĖįŅųČÜŅŗ
¼ÓČė×ćĮæĻ”ĻõĖį£¬ŌŁ¼ÓČė×ćĮæµÄĻõĖįŅųČÜŅŗ
£»
¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘĮæ³ĮµķµÄÖŹĮ棻¼ĘĖć³öĀČ»ÆÄʵÄÖŹĮ棬ŌŁµĆѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹż£®

 £Ø2013?Ī«·»£©Ä³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖ²ā¶Ø“æ¼īѳʷ£Øŗ¬NaClŌÓÖŹ£©ÖŠĢ¼ĖįÄĘÖŹĮæ·ÖŹżµÄŹµŃé·½°ø£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø2013?Ī«·»£©Ä³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖ²ā¶Ø“æ¼īѳʷ£Øŗ¬NaClŌÓÖŹ£©ÖŠĢ¼ĖįÄĘÖŹĮæ·ÖŹżµÄŹµŃé·½°ø£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø