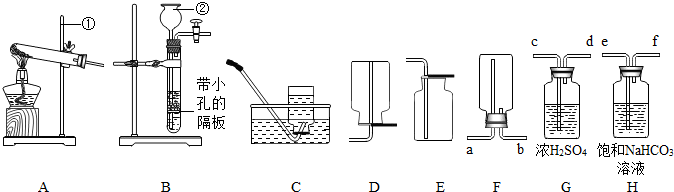
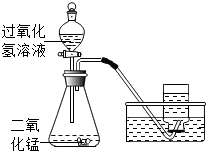
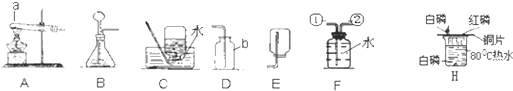
��������װ�ã������ѧ��ѧ֪ʶ�ش��������⣮
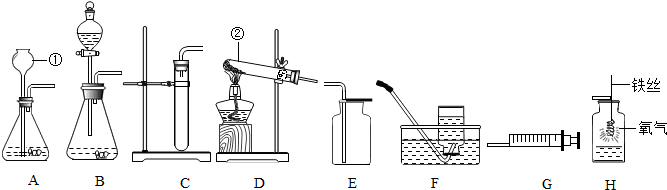
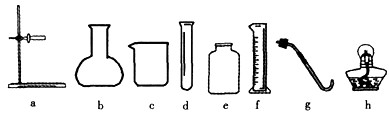
��1����д��ͼ�б�����������ƣ���
����©��
����©��
����
�Թ�
�Թ�
��
��2��ʵ�����ù���������ȡ��������ʱ������װ�����ѡ��
C
C
���ռ�װ��ѡ��
E��F
E��F
��
������ʱ�������������������ԼҩƷ������װ�����ѡ��
B
B
�����ţ���д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��
��
��3��ʵ�����ø��������ȡ����ʱ������װ��Ӧѡ��
D
D
���ţ���д���䷴Ӧ�ı���ʽ
��
��4������Eװ���ռ�O
2������O
2�Ƿ��ռ����ķ�����
�������ǵ�ľ������ƿ�ڣ�ľ����ȼ����
�������ǵ�ľ������ƿ�ڣ�ľ����ȼ����
��
��5����ͼH����˿�������о���ȼ�գ�
��������
��������
�����ɺ�ɫ���壬��ƿ��Ԥ�ȷ�������ˮ��Ŀ����
��ֹȼ�����ɵĸ����ۻ��ヲ��ƿ�ף�ʹ����ƿը��
��ֹȼ�����ɵĸ����ۻ��ヲ��ƿ�ף�ʹ����ƿը��
��
��6��ע����G�����ڼ��װ��A�������ԣ��������£�
������ƿ�м�������ˮ��
��û����©���¶�
��û����©���¶�
����
�ڽ�ע����C���ӵ�װ��A�ĵ��ܿڴ���
�ۻ�������ע����G�Ļ������۲쵽
����©���¶��������ݳ�
����©���¶��������ݳ�
����ʾװ��A�����������ã�
��7��ʵ������װ��A��ȡ����ʱ������ע����G�滻����©�����ŵ���
���Կ��Ʒ�Ӧ������
���Կ��Ʒ�Ӧ������
��
��8������װ��F�ռ���������������ԭ������ǣ���д����ԭ��
��
���Ⱥ������ռ�����
���Ⱥ������ռ�����
����
����ƿ��δװ��ˮ��������
����ƿ��δװ��ˮ��������
��
��9����ѧ��ʵ����ϣ�С���ø��������ȡ���ռ���һƿ��������dz��ɫ������ϸ��˿ȼ��ʵ��ʱ��δ��ϸ��˿ȼ�գ���С���쳣�˷ܣ�ʵ��ɹ��ˣ���ʵ����������˼���ƿ���������ߵ�����ʦ�ԣ�˵���ҵļ���ƿ���ˣ�������λͬѧʵ������г��ֵ����⣮
С�֣���
�Թܿ�û������
�Թܿ�û������
����
��˿���������˶�δ��ĥ��ȥ���������ɣ�
��˿���������˶�δ��ĥ��ȥ���������ɣ�
��
С�죺
����ƿ��û��Ԥ��������ˮ���һЩɳ��
����ƿ��û��Ԥ��������ˮ���һЩɳ��
��

 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�



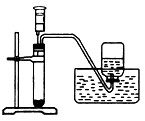
 ʵ�����ù������⣨H2O2����Һ���׳�˫��ˮ����ȡ������װ����ͼ����ش��������⣮
ʵ�����ù������⣨H2O2����Һ���׳�˫��ˮ����ȡ������װ����ͼ����ش��������⣮