
| A. | 生活污水任意排放会污染环境 | B. | 水由氢分子和一个氧原子构成 | ||
| C. | 水是取之不尽,用之不竭的资源 | D. | 硬水经过滤可以转化为软水 |
分析 A.根据水的三大污染源进行分析判断;
B.根据水的宏观组成进行分析判断;
C.根据水资源状况进行分析判断;
D.根据降低水硬度的方法进行分析判断.
解答 解:A.生活污水任意排放会污染环境,故A正确;
B.水从宏观来讲是由氢元素和氧元素组成的,一个水分子从微观来讲是由两个氢原子和一个氧原子构成的,故B不正确;
C.地球上水资源虽然很丰富,但淡水资源不足,不是取之不尽,用之不竭的资源,故C不正确;
D.硬水经过过滤不能除去水中的可溶性钙、镁化合物,故不能降低水的硬度变成软水,故D不正确.
故答案为A.
点评 此题考查学生对于水的组成、水的污染以及水的净化、硬水软化等知识点的考查,掌握相关知识是解题的关键.


科目:初中化学 来源: 题型:解答题
 如图标出的是灭火器的组成物质,请回答下列问题.
如图标出的是灭火器的组成物质,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X中氮元素的化合价为+4价 | B. | X是氧化物 | ||
| C. | X的稀溶液能使紫色石蕊试液变红 | D. | X中氮、氧元素的质量比为1:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
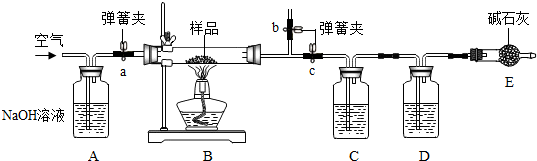
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 永春老醋是中国四大名醋之一.它是以优质糯米、红粬、芝麻、水等为原料,用独特配方、精工发酵、陈酿多年而成,具有色泽棕黑、酸中带甘、醇香爽口、久藏不腐等特点,既是质地优良的调味品,又兼有治病妙用,可防治腮腺炎、胆道蛔虫、感冒等疾病.
永春老醋是中国四大名醋之一.它是以优质糯米、红粬、芝麻、水等为原料,用独特配方、精工发酵、陈酿多年而成,具有色泽棕黑、酸中带甘、醇香爽口、久藏不腐等特点,既是质地优良的调味品,又兼有治病妙用,可防治腮腺炎、胆道蛔虫、感冒等疾病.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
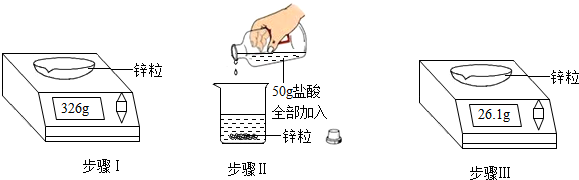
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com