
金属材料在工业上有广泛的用途。
(1)铝合金材质与纯铝比较,主要优点是 ;
(2)钢铁的锈蚀主要是铁与空气中的 共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 ;
(3)为了避免钢铁腐蚀,通常在钢铁外壳上镶嵌比铁活动性强的金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图的两个实验: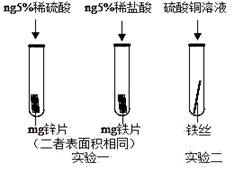
①实验一,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 ;②实验二,若出现 现象,可证明铁的活动性强于铜,该反应的化学方程式为 。
(1)强度大(或“质轻”等 ) ;(2)氧气和水; Fe2O3+6HCl═2FeCl3+3H2O;
(3)①选取的酸的种类不同 ; ②铁丝表面出现红色物质 ; Fe + CuSO4 = FeSO4 + Cu
解析试题分析:(1)依据合金的特性,铝合金材质与纯铝比较,强度大、质量轻;(2)钢铁的锈蚀,实际上是铁跟水和氧气共同作用的结果;铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水;(3)①从图示可以看出选取的酸的种类不同,因此以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱不够合理;②实验二中,若铁丝表面出现红色物质,溶液由蓝色变成浅绿色,可证明铁的活动性强于铜.
考点:合金与合金的性质;金属活动性顺序及其应用;金属锈蚀的条件及其防护;书写化学方程式、文字表达式、电离方程式


科目:初中化学 来源: 题型:填空题
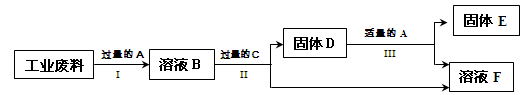
A~D是初中化学所学的常见物质,其转化关系如右图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C、D均为黑色粉末。请回答下列问题:
(1)写出反应②的化学方程式:
(2)反应③的基本反应类型是:
(3)物质A的一种用途
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(7分)金属与我们生活息息相关,按要求回答问题。
(1)下列物质属于合金的是 。
| A.氧化铁 | B.不锈钢 | C.黄铜 | D.硫酸铜 |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(7分)铁和铜是生产生活中常见的金属.
(1)能有效防止铁制品生锈的措施是_______
| A.家用水龙头镀铬 | B.汽车表面喷漆打蜡 |
| C.自行车链条涂油 | D.菜刀用后洗净擦干 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
比较和归纳是学习化学的常用方法。某学习小组的同学在下图所列出的实验装置的基础上进行了学习。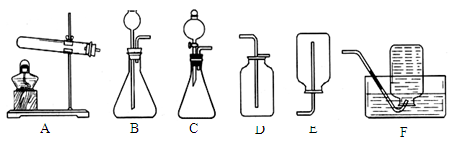
(1)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为 ,可用B装置还可制取另一气体,写出发生装置中的化学方程式是 。
(2)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,微溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 。
(3)如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题: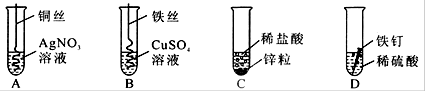
①写出B中反应的化学方程式: 。
②要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是 (填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
某同学设计的“用氧化铜制取铜”的实验步骤是:
第一步:取少量氧化铜粉末放入小烧杯中,然后加入适量稀硫酸,微热;
第二步:向上面的溶液中加入过量的铁粉,充分搅拌;
第三步:过滤烧杯中的物质,滤纸上的物质是A,滤液中的溶质是B;
第四步:将物质A移入小烧杯中,加入过量的C溶液,充分反应后过滤。
请回答下列问题:
(1)第一步实验中观察到的实验现象是 ;该反应的化学方程式为 。
(2)第三步实验中滤纸上A是 ,滤液中B是 ;
(3)第四步实验中加入过量的C溶液是 ,其目的是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
等质量的三种金属A、B、C和相同质量分数的足量稀硫酸反应, 都生成+2价金属硫酸盐,其反应情况如图所示。依图可知三种金属的活动性顺序是 ,它的相对原子质量大小的顺序是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
现有银、铜、铁三种金属,某研究小组为探究银、铜、铁的金属活动性顺序,设计了三
个实验:(Ⅰ)将铁片浸入稀硫酸中;(Ⅱ)将银片浸入稀硫酸中;(Ⅲ)将铁片浸入硫酸铜溶液中。
实验(Ⅲ)中反应的化学方程式为 ;该反应的基本类型为 反应
上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象) 。根据以上探究,三种金属的活动性由强到弱的顺序是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
事物都具有两面性。如:CO可作冶金工业原料,却对人体健康有害;O2可用于急救病人,维持生命活动需要,却参与钢铁的锈蚀过程。
(1)写出高炉炼铁中CO还原氧化铁的化学反应方程式: ;
(2)金属材料包括纯金属以及它们的合金,黄铜(含铜和锌)、生铁都属于 。钢和生铁由于 元素含量的不同,使得钢和生铁的坚韧性有较大差异。
(3)将黄铜和生铁分别放人足量的稀盐酸中,浸泡后都有残留固体,其中一种固体一定含 ,另一种固体一定含 。
(4)铁浸泡在盐酸中发生反应的化学方程式为 , 该反应的基本类型是 。
(5)食品包装中,有一些是用铁粉做双吸剂,铁粉既可以防腐又可以保持食品干燥,是因为铁粉能吸收空气中的 和 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com