
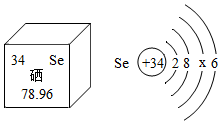
 硒元素的部分信息如图所示.下列说法错误的是( )
硒元素的部分信息如图所示.下列说法错误的是( )| A. | 硒是非金属元素 | |
| B. | 硒元素的质子数为 34 | |
| C. | 硒的原子结构示意图中 x=18 | |
| D. | 在化学反应中,硒原子容易失去 2 个电子 |
分析 根据图中元素周期表可以获得的信息:原子序数、元素种类等,原子序数=质子数,当质子数=核外电子数,为原子;进行分析判断即可.
解答 解:A、根据元素周期表中的一格中获取的信息,该元素的名称是硒,属于非金属元素,故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为34,又原子序数=质子数,因此硒元素的质子数为34,故选项说法正确.
C、当质子数=核外电子数,为原子,由硒的原子结构示意图,则34=2+8+x+6,解得x=18,故选项说法正确.
D、由硒的原子结构示意图可知,原子最外层电子数为6,在化学反应中,硒原子容易得到2个电子形成稳定结构,故选项说法错误.
故选D.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法、原子中核内质子数和核外电子数之间的关系等进行分析解题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 用燃烧法可以区分羊毛和尼龙线 | |
| B. | 油脂不溶于水,易溶于汽油等有机溶剂 | |
| C. | 蛋白质遇可溶性重金属盐会失去生理活性 | |
| D. | 葡萄糖在人体内可转化为蔗糖、淀粉和纤维素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
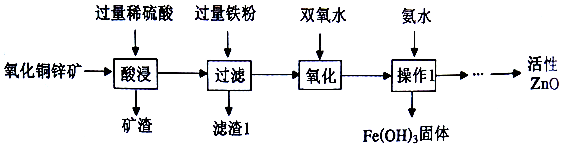
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
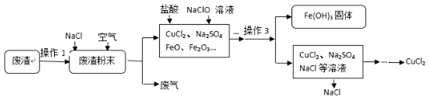
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 试管:我被摔碎了 | |
| B. | 铁钉:我在潮湿空气中最容易生锈啦 | |
| C. | 灯泡:我通电后发光了 | |
| D. | 蜡烛:我受热融化,遇冷又凝固了 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸和碱之间发生的反应不一定是中和反应 | |
| B. | 工业冶炼铝和生产生石灰的反应类型相同 | |
| C. | NH4NO3中氮元素的化合价相同 | |
| D. | CO${\;}_{3}^{2-}$离子也能使酚酞试液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
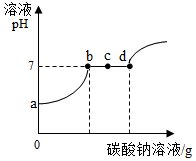 酸、碱、盐在我们的生活中有着重要作用.
酸、碱、盐在我们的生活中有着重要作用.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com