
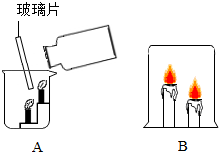
 观察如图所示的实验,回答问题:
观察如图所示的实验,回答问题:分析 (1)因为二氧化碳的密度比空气的大,所以可以像倾倒液体一样倒入烧杯中,二氧化碳不燃烧,也不支持燃烧;因此下层蜡烛先被熄灭,上层后被熄灭.
(2)根据实验现象可以判断正确的逃生方法.
解答 解:(1)观察两支蜡烛的变化,因为二氧化碳的密度比空气的大,所以下面的蜡烛火焰先熄灭,上面的蜡烛火焰后熄灭.这个实验说明了:CO2的密度比空气的密度大;CO2不能燃烧也不支持燃烧.故填:低处的蜡烛先熄灭,高处的蜡烛后熄灭.原因是CO2密度比空气大,聚集在烧杯底部,所以低处蜡烛先熄灭.
(2)由以上实验的现象可知,用湿毛巾捂住鼻子既可以防止烟尘进入呼吸道,又可以降低空气的温度;沿墙角伏低身子迅速爬向门外可以防止二氧化碳造成的窒息.
故填:用湿毛巾捂住口鼻,匍匐前进,寻找安全出口.
点评 本题主要考查物质的组成、性质和用途等方面的知识,特别是能够从实验现象中得到启示--即正确的逃生方法.


科目:初中化学 来源: 题型:解答题
| 菜肴 | 半小时 | 6小时 | 18小时 | 24小时 |
| 炒青菜 | 0.6861 | 0.7982 | 4.3333 | 5.3624 |
| 韭菜炒蛋 | 1.8153 | 1.9249 | 2.8390 | 5.6306 |
| 红烧肉 | 2.4956 | 4.2558 | 4.3668 | 5.5188 |
| 红烧鲫鱼 | ---- | 2.0948 | 3.2300 | 7.2397 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有碳酸根(CO32-)离子 ②样品中含有铜(Cu2+)离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①Fe+H2SO4═H2↑+FeSO4 ②Fe+CuSO4═Cu+FeSO4 (均用方程式表示) |

| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com