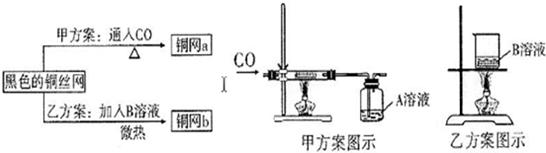
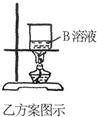
实验小组的同学发现:加热铜与浓硫酸的混合物,能生成一种无色有刺激性气味的气体和蓝色溶液.
(1)①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐.
②硫酸铜溶于水后,溶液呈酸性.铜、银(能、不能)与稀硫酸、盐酸反应产生氢气.
(2)①对于生成的蓝色溶液,小东认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而可能是硫酸铜溶液,小楠的理由是.
②写出铜与浓硫酸共热的化学方程式.
③小东根据化学方程式说,该方法适用于以铜为原料大量制取硫酸铜,小田认为不适宜,你能说出小田的一个理由吗?.
(3)【提出问题】上述蓝色溶液中有无硫酸剩余?
(4)【实验论证】小坤认为可向蓝色溶液中滴加氯化钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是.
(5)【反思评价】
①有同学提问:为什么不可以用石蕊试液来进行检验?你的回答是
.
②同学们发现:将足量的铜和足量的浓硫酸置容器中加热,反应一段时间后,反应会逐渐变慢,最后反应停止,你能说出反应停止的原因吗.
【答案】
分析:在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液(除稀硝酸)反应生成氢气;注意分析题中提供的资料信息:①某些不活泼的金属(如铜)能与一些强氧化性的酸(如浓硫酸)发生反应,生成水而不生成氢气,同时生成二氧化硫和铜盐;②硫酸铜溶于水后,溶液呈酸性.
解答:解:(1)由于银和铜都在氢后,因此都不能和稀硫酸、盐酸反应生成氢气,故答案为:不能
(2)①根据质量守恒定律中的元素种类在化学变化前后不变,生成的蓝色溶液是金属铜和浓硫酸反应生成,因此该蓝色溶液不可能时硝酸铜溶液,故答案为:反应前后元素种类不变
②由于金属和浓硫酸在加热条件下生成水、二氧化硫和硫酸铜,故答案为:Cu+2H
2SO
4
CuSO
4+2H
2O+SO
2↑
③由于二氧化硫气体是一种有刺激性气味的有毒气体,是造成空气污染的主要气体之一,因此不能用金属铜和浓硫酸反应来制取大量的硫酸铜,故答案为:生成的二氧化硫会污染环境
(4)由于硫酸铜中也含有硫酸根离子,也能和氯化钡溶液反应生成白色沉淀,因此不能用氯化钡溶液来验证硫酸溶液是否有剩余,故答案为:硫酸铜中也含有硫酸根离子,也能和氯化钡溶液反应生成白色沉淀
(5)①根据提供的资料不难看出,硫酸铜溶液也是酸性溶液,也能使紫色石蕊试液变红,故答案为:硫酸铜溶液也是酸性的
②由于随着反应的进行,浓硫酸中的溶质越来越少,即浓硫酸逐渐的变成了稀硫酸,而稀硫酸和金属铜不反应,所以反应会越来越慢直至停止,故答案为:随着反应的进行,浓硫酸中溶质的质量分数逐渐变小,稀硫酸与铜不反应
点评:本题难度较大,主要考查了金属的有关的化学性质,从中培养学生分析资料、解决问题的能力.

 CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑