
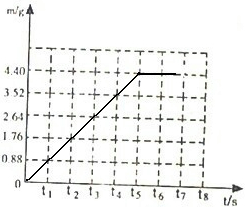
 小明同学将12.5g含杂质的石灰石样品与100g足量的稀盐酸相混合(石灰石中的杂质不参加反应),充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示
小明同学将12.5g含杂质的石灰石样品与100g足量的稀盐酸相混合(石灰石中的杂质不参加反应),充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
| 100 |
| 44 |
| x |
| 4.4g |
| 10g |
| 12.5g |


科目:初中化学 来源: 题型:
 (2012?静安区一模)鸡蛋壳的主要成分是碳酸钙,小明同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下的探究实验,请你参与他的活动.
(2012?静安区一模)鸡蛋壳的主要成分是碳酸钙,小明同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下的探究实验,请你参与他的活动.| 其质量不再减少 |
| 0.1mol×100g/mol |
| 12.5g |
| 0.1mol×100g/mol |
| 12.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | l | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液的浓度 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/g | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
查看答案和解析>>
科目:初中化学 来源: 题型:
鸡蛋壳的主要成分是碳酸钙,小明同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下的探究实验,请你参与他的活动。
【实验过程】将鸡蛋壳洗净、干燥、称量并捣碎后放入到锥形瓶中,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应,反应生成的气体全部逸出)。
【实验数据】鸡蛋壳12.5g + 稀盐酸40.5g  剩余的混合物48.6g
剩余的混合物48.6g
【数据处理】① 根据质量守恒定律,计算反应生成二氧化碳的质量为 (25) g。
② 通过化学方 程式计算鸡蛋壳中含碳酸钙的物质的量解题过程: (26)
程式计算鸡蛋壳中含碳酸钙的物质的量解题过程: (26)
③ 计算鸡蛋壳中碳酸钙的质量分数解题过程: (27)
【误差分析】实验中,如有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比 (28) (填写“偏大”、“偏小”或“不变”)。

查看答案和解析>>
科目:初中化学 来源:2013年上海市静安区中考化学一模试卷(解析版) 题型:解答题
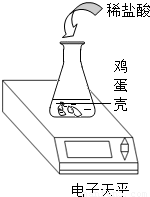 鸡蛋壳的主要成分是碳酸钙,小明同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下的探究实验,请你参与他的活动.
鸡蛋壳的主要成分是碳酸钙,小明同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下的探究实验,请你参与他的活动. 剩余的混合物48.6g
剩余的混合物48.6g查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com