
【题目】化学是从微观角度研究物质的组成、结构及变化的科学,构成物质的粒子之间的关系如图1所示,请回答下列问题:

(1)甲是_____.
(2)氢气、金刚石、硫酸铜三种物质中,由离子构成的物质是_____.
(3)图2是氟元素的原子结构示意图,方框横线上的数字是______.
(4)在化学变化前后一定发生改变的是______(填字母).
A 元素的种类 B 原子的个数 C 原子的质量 D 分子的种类
(5)氟元素和氢元素形成的化合物的水溶液叫氢氟酸(HF),可用于雕刻玻璃,其主要原因是氢氟酸和玻璃的主要成分二氧化硅发生反应,生成四氧化硅气体和水,写出该反应的化学方程式_____.
【答案】原子 硫酸铜 7 D ![]()
【解析】
(1)据图可以看出,分子分解可得到甲,甲可以结合形成分子,且甲可通过得失电子形成离子,故甲是原子,故填:原子;
(2)在氢气、金刚石、硫酸铜三种物质中,硫酸铜是由铜离子和硫酸根离子构成的,氢气是由氢分子构成的,金刚石是由碳原子构成的,故填:硫酸铜;
(3)原子的核内质子数=原子的核外电子数,图2方框横线上的数字是9-2=7;
(4)根据质量守恒定律,化学反应前后,原子的种类、数目、质量不变,故元素的种类、原子的个数、原子的质量都不会改变,而化学反应的实质是分子分成原子、原子重新组合成新物质的分子,在化学变化前后一定发生改变的是分子的种类。故选D;
(5)氢氟酸与玻璃的主要成分二氧化硅发生反应,生成四氟化硅气体和水,反应的化学方程式为:![]() 。
。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:初中化学 来源: 题型:
【题目】关于下列符号或图示的说法正确的是( )
①![]() ②
②![]() ③
③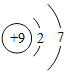 ④
④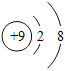 ⑤
⑤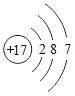 ⑥
⑥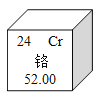
A.①表示两个氧原子
B.由⑥可知铬的相对原子质量为52.00g
C.②和④均表示阳离子
D.③和⑤表示的元素在形成化合物时通常显-1价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乐融和张炎帮助老师探究中和反应的实验,操作如图所示,请同学们完成以下问题:
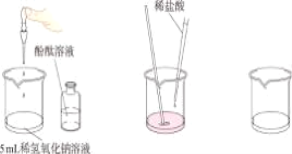
(1)实验中发生反应的化学方程式_____。
(2)向乐融加入了适量的混有酚酞溶液的氢氧化钠溶液中,边滴加稀盐酸边用玻璃棒不断搅拌,当看到_____现象,证明氢氧化钠和稀盐酸发生化学反应了。
(3)乐融同学对最终变为无色的溶液的成分很感兴趣,他猜测溶液中的溶质除酚酞外一定有_____可能有_____(填化学式)为了最终确定溶液的成分,马墩墩同学设计方案,取少量反应后的试剂向其中加入适量硝酸银溶液,如果看到白色沉淀,就能证明可能有的物质一定存在。请同学们对该方案评价_____。张炎提出另外一种方案,取反应后的少量试剂于试管中,向其中加入了适量的碱_____(填化学式)产生了明显的实验现象,最终确定的溶液的成分。
(4)同学们最后总结,可以根据明显的现象证明是否有其他物质生成,也可以根据明显的现象_____来判断化学反应是否发生。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是全球最大太阳能飞机“阳光动力2号”。
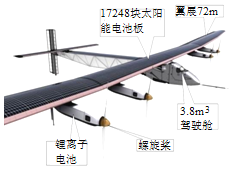
“阳光动力2号”的机身和机翼均采用碳纤维复合材料制成,该机的机翼、机身和水平尾翼上共贴敷了17248 片135pμm厚的单晶硅薄膜太阳能电池。请回答下列问题:
(1)碳纤维复合材料是有机纤维经过一系列热处理转化而成,含碳量高于90%,其强度比钢高五倍,重量却不到钢的一半。碳纤维复合材料具有的优良性能是________(填字母)。
A 硬度大、密度大
B 密度小、熔点低
C 密度小、强度高
(2)太阳能电池芯片的常用材料是“单晶硅”。硅的元素符号是①_______,高纯硅常用作半导体材料,这说明硅具有②_________性。
(3)制造该飞机时常用乙炔( C2H2)进行焊接。实验室可以用电石( CaC2 )和水反应制得乙炔气体,同时生成一种碱。该反应的化学方程式为①__________,电石中碳元素的化合价是②________。
(4)太阳能飞机与用航空煤油做燃料的飞机相比,不仅可以节约_______,还可以减少对空气的污染。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)已知A~G七种物质都是初中化学课本中出现过的化合物,其中F是常用的建筑材料;H为常见的单质。各物质之间存在如下转化关系(反应条件如下图所示)。
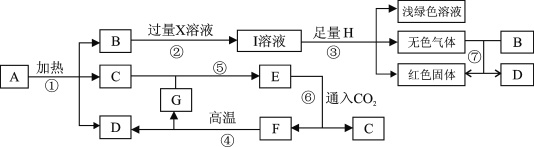
(1)上述I溶液中的溶质有 ;
(2)写出反应①的化学方程式 ;
(3)写出在①~⑦反应中属于复分解的方程式是 ;
写出在①~⑦反应中属于化合反应的方程式是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A﹣H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应;B是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
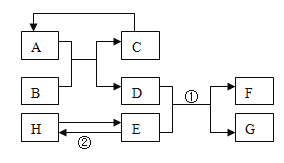
(1)C的化学式:______.
(2)写出一个符合反应②的化学方程式______.
(3)我国工业制硫酸的第一步反应是硫铁矿(主要成分为FeS2)即FeS2与氧气在高温条件下反应生成B和二氧化硫,写出该反应的化学方程式______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中常用的实验装置,请回答下列问题。

(1)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为______,可选择的发生装置为____(填字母)。
(2)实验室用石灰石和稀盐酸制取CO2的原理是____________(写化学方程式),可选用上述装置_________(填序号)制取CO2。该反应生成的二氧化碳中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的________口(填“①”或“②”)通入。
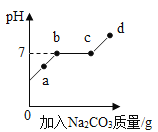
(3)在制取二氧化碳反应装置的残液中加入Na2CO3溶液,溶液pH变化如图所示(提示:氯化钙溶液呈中性)。a点时,溶液中的溶质的化学式是_________。bc段溶液pH一直为7的理由是_____________(写化学方程式)。滴入Na2CO3溶液的过程中观察到的现象依次是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】双氧水常用于消毒、漂白等,它是过氧化氢(![]() )的水溶液。含过氧化氢30%的溶液以二氧化锰为催化剂可以迅速分解放出氧气,发生反应的化学方程式为:
)的水溶液。含过氧化氢30%的溶液以二氧化锰为催化剂可以迅速分解放出氧气,发生反应的化学方程式为:![]()
![]()
![]() ,现欲制得干燥而又纯净的氧气,可采用下图实验装置进行。
,现欲制得干燥而又纯净的氧气,可采用下图实验装置进行。

其中装置Ⅰ中,锥形瓶内盛的是二氧化锰,分液漏斗内盛的是30%的过氧化氢溶液,请回答:
(1)装置Ⅱ中的化学药品是_____,作用是_____。
(2)装置Ⅲ可用来检验氧气是否干燥,其中盛放的化学药品是_____,证明所得氧气已经干燥了的现象是_____。
(3)装置Ⅳ中氧气是否收集满的检验方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其他成分可溶于水但不参与反应)。
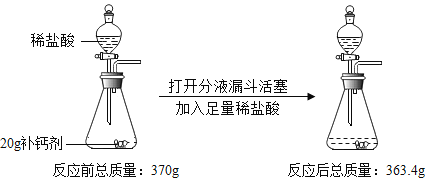
(1)生成二氧化碳的质量为__________g。
(2)计算该补钙剂中碳酸钙的质量分数_________。
(3)该实验中,装置的气密性对测定结果______(填“有”或“无”)影响。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com