
【题目】加热某白色固体A与二氧化锰混合物,产生一种无色无味的气体B和另外一种固体物质;取淡黄色粉末C点燃放入B中,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体D,试回答:
(1)写出上述物质的名称: A__________,B_________,C________,D_______;
(2)写出A反应的文字表达式:______________________________,属于______反应;
(3)写出C在A中的文字表达式:___________________________,属于______反应。
科目:初中化学 来源: 题型:
【题目】如图所示,关闭止水夹a、b、c,使过量的红磷和木炭分别在盛有空气的等容积的甲、乙两瓶中同时燃烧,试回答
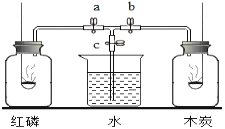
(1)燃烧停止并冷却,若打开止水夹a、c后观察到的现象是_____;原因是_____。
(2)若打开止水夹b、c后观察到的现象是_____;原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从下列常见仪器图示中,选择恰当的字母序号填空:
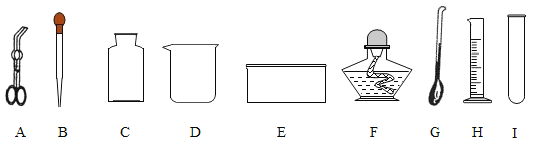
(1)可以直接在酒精灯火焰上加热的玻璃仪器是____;
(2)镁条燃烧时,用来夹持镁条的仪器是____;
(3)用酒精灯加热时需要垫上石棉网的仪器是____;
(4)取用粉末状固体药品用到的仪器是____;
(5)吸取和滴加少量液体试剂的仪器是____;
(6)量取8mL稀硫酸,应选用的仪器是 _____ 和_______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用如图1装置,小卫设计并实施了下列实验,(压强传感器用于测量抽滤瓶内压强变化:各数据均于同温下测定获得)
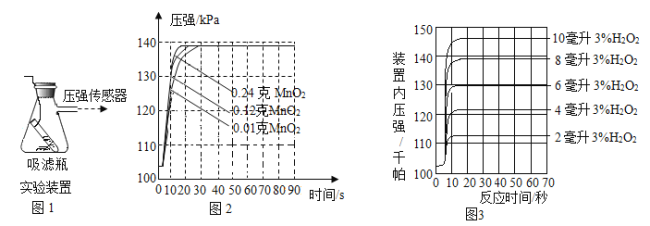
实验Ⅰ:再小试管中加入8mL溶质质量分数为3%的双氧水(ρ=1g/mL),在抽滤瓶中分别加入不同质量的MnO2,使其反应并启动传感器,记录容器内压强变化于图2中.
实验Ⅱ:在抽滤瓶中加入0.1g MnO2,在小试管中分别加入不同体积溶质质量分数为3%的双氧水,使其反应并启动传感器,记录容器内压强变化于图3中.
请根据以上实验回答下列问题:
(1)使容器内压强增大的反应的文字表达式:_____________________;
(2)根据图2可发现,该实验条件下,30s内催化分解8mL溶质质量分数为3%的双氧水,MnO2的最小用量为______________g;
(3)根据图3可发现,0.1g MnO2至少能快速催化分解__________g过氧化氢;
(4)根据图2与图3可发现,MnO2的用量总体上与O2产量_____________(填“正相关”、“不相关”或“负相关”),根据图3还可发现,该试验中,O2产量总体上与双氧水用量是___________(填“正比”或“反比”);
(5)下列因素中,与本实验所测数据的精确度有关的是__________ 。
A 反应容器的气密性 B 称量MnO2质量的精准度 C 量取双氧水体积的精准度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A的无色溶液与黑色固体B常温混合反应,生成无色气体C;另一种黑色固体D能在C中燃烧,生成能使澄清石灰水变浑浊的气体无色气体E;如把黄色粉末F点燃后放入盛C的集气瓶中,能剧烈燃烧,生成一种无色有刺激性气味的气体G。请回答:
(1)写出下列物质的名称或化学式:A ,B ,F 。
(2)写出D在C中燃烧的文字表达式 ;基本反应类型是 。
(3)写出F在C中燃烧的文字表达式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学收集到一瓶浑浊的河水,带回实验室进行如图所示的实验
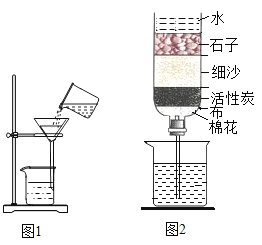
(1)实验中常加入明矾,其作用是______,过滤时常用________做过滤层,在生活中还可以用_______代替;
(2)图1实验缺少的一种仪器是_____其作用是_______;
(3)过滤后,发现滤液仍然浑浊,造成这一现象的操作可能是________(一条即可);
(4)对实验改进后,重新过滤后得到略带红色的澄清液体。如果要除去水的颜色,可利用的物质是________________;
(5)如图2是同学们制作的一种简易净水器,利用该装置处理河水得到无色透明的液体,活性炭起________作用,通过该装置__________(填“能或不能”)降低水的硬度,生活中常采取_____方法降低水的硬度;
(6)图1和图2实验后得到的水______(填“能或不能”)代替蒸馏水用于实验,请说明理由___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在小英家的仓库里,堆放着一袋袋化肥一一碳酸氢铵( NH4HCO3).过了一个夏天,小英发现这种化肥所持有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了,检查发现变少的化肥包装袋没有密封,化肥也没有撒落在地上,更没有人进过仓库开袋使用。
为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味.粉末为什么会消失呢?
(1)(提出问题)碳酸氢铵粉末消失的原因是什么?
(2)(猜想)①碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态。②碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和一些氧化物。
(3)(查阅资料)①碳酸氢铵属于氨肥,不具有升华的性质,说明上述猜想__________ (填序号)不成立;②氨气(化学式NH3)具有特殊的刺激性气味,极易溶于水,其水溶液是碱性,但干燥的氨气不能使干燥的红色石蕊试剂变蓝;③NO2为红棕色气体。NO为无色气体,在空气中易发生反应:2NO+O2=2NO2
(4)(实验操作,现象与结论)
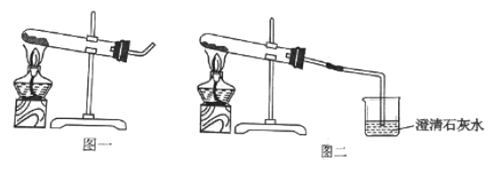
实验操作 | 实验现象 | 实验结论 |
①取适量碳酸氢铵于试管中加热,如图一所示,将干燥的红色石蕊试纸接近导管口 | 产生强烈的刺激性气味,试管壁上有无色液滴且试纸变蓝,但未见红棕色气体 | 分解产物中有______,没有__________ |
②按如图二所示装置继续实验,直到反应完全 | 澄清石灰水变浑浊 | 分解产物中有__________ |
(5)(应用)①利用氨气的化学性质,请写出实验室检验氨气的方法(写出实验操作、现象、结论):________________________________________;
②如果你家里有碳酸氢铵化肥,你应该如何保存? ______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com