
分析 (1)根据质量守恒定律计算参加反应的氧气的质量;
(2)根据 CO2和 H2O 的质量计算化学计量数之比;
(3)根据,24g CH4完全燃烧所需氧气的量计算
解答 解:(1)根据质量守恒定律,参加反应的氧气的质量为:54g+22g+28g-24g=80g;
(2)化学方程式中 CO2和 H2O 的化学计量数之比为:$\frac{22g}{44}:\frac{54g}{18}$=1:6;
(3)设24g CH4完全燃烧所需氧气的质量为x
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
16 64
24g x
$\frac{16}{64}=\frac{24g}{x}$
x=96g
故需增加氧气的质量为:96g-80g=16g
故填:80;1:6;16
点评 本题考查学生利用化学反应方程式的计算,并注意计算格式的规范.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 属于一种氧化物 | |
| B. | 1个胡萝卜素分子由40个碳原子、26个氢分子和2个氧分子构成 | |
| C. | 碳、氢、氧三种元素的质量比为:40:52:4 | |
| D. | 其中碳元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用碳酸氢钠的发酵粉可焙制糕点 | B. | 用肥皂水可区分硬水和软水 | ||
| C. | 利用洗洁精的乳化作用可洗净餐具 | D. | 用工业酒精可兑制饮用酒 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
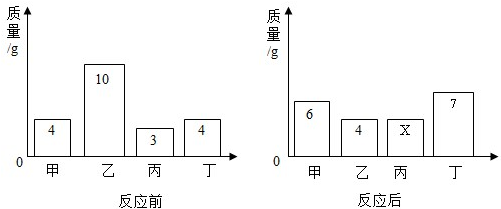
| A. | 反应后丙的质量为 4g | B. | 该反应为分解反应 | ||
| C. | 生成的丙、丁的质量之比为1:3 | D. | 乙的相对分子质量是甲的3倍 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
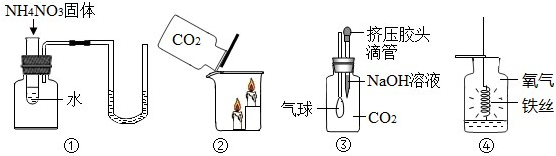
| A. | 图①中 U 形管内液面左高右低 | B. | 图②中的蜡烛自下而上依次熄灭 | ||
| C. | 图③中小气球变瘪 | D. | 图④中的铁丝剧烈燃烧,火星四射 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取少量滤液B于试管中,滴 加几滴无色酚酞,振荡,观察现象 | 溶液无明显现象 | 猜想三不成立 |
| 步骤二:取少量滤液B于试管中,滴 加适量NaOH溶液,振荡,观察现象 | 产生白色沉淀 | 猪想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KMnO4、CuCl2、Fe2(SO4)3 | B. | HCl、AgNO3、Na2SO4 | ||
| C. | NaCl、KNO3、(NH4)2SO4 | D. | H2SO4、K2CO3、NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com