
【题目】某同学在做“硫在氧气中燃烧”的实验时,为了防止空气污染,用氢氧化钠溶液来吸收二氧化硫。下面是该同学实验与计算过程:
(1)配制100g溶质质量分数为10%的氢氧化钠溶液,需用天平称取______g的氢氧化钠;配制上述溶液,可用20%氢氧化钠溶液______g加水稀释。
(2)如下图所示,硫燃烧后,注入所配制的NaOH溶液吸收二氧化硫。若集气瓶中生成0.64g的二氧化硫,将其完全吸收,针筒要吸取的氢氧化钠溶液中含氢氧化钠___克。(假设NaOH溶液吸收SO2 时只发生如下反应:SO2+2NaOH=Na2SO3+H2O)

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
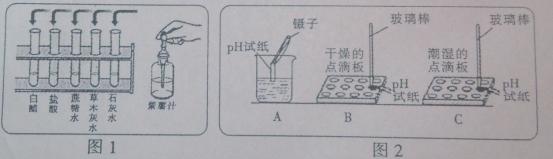
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作有:①过滤;②蒸发结晶;③加过量Na2CO3溶液;④加过量NaOH溶液;⑤加过量稀盐酸;⑥加过量BaCl2溶液。
(1)请用以上序号排序_________设计实验,完全除去氯化钠中可溶性杂质。
(2)请解释除去Na2SO4时的反应原理_________(用化学方程式表示)。
(3)过滤后若滤液浑浊,请写出一条可能的原因_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是( )
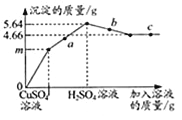
A. a点对应溶液pH>7
B. b点对应溶液中溶质有2种
C. m=3.31
D. 取c点对应溶液,滴加NaOH溶液,立刻产生沉淀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为甲乙两物质的溶解度曲线,下列说法正确的是( )
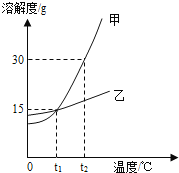
A. 甲的溶解度大于乙的溶解度
B. t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
C. t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克
D. 要使接近饱和的乙溶液转化为饱和溶液,可以采用降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】固体物质A、B的溶解度曲线如右图所示,①②③④是分别用100g水配制的不同状态下A溶液,下列说法正确的是:
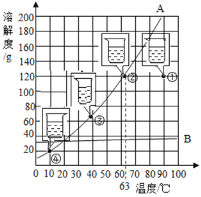
A. 状态①溶液不饱和,状态②③④溶液饱和
B. 60℃时A、B的饱和溶液降温至10℃时析出晶体质量A>B
C. 除去A中少量的B,常采用蒸发结晶的方法
D. ④的溶液质量分数最小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酱油是中国的传统调味品。酱油中主要含有水、糖类、蛋白质、氯化钠等,富含铁、硒、钙等元素。请用化学用语填空:
(1)酱油中一种微量元素_____。
(2)钙离子_____。
(3)氯化钠中钠元素的化合价_____。
(4)(写出加点部分的化学用语)蛋白质中含有氯元素_____。
(5)一个水分子中含有两个氢原子_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】.如图所示,A~H 分别是氢、氧、硫、氯、钠、铜、钙、铁八种元素中的两种或几种组成的初中化学常见物质。“→”箭头表示物质间能转化,“—”表示物质间能反应),G 用于配制“波尔多液”,溶液显蓝色。请回答:

(1)G 的化学式为_____。
(2)C→D 的实验现象为:_____。
(3)写出下列化学方程式:
A→B:_____。
G→H:_____。
(4)在上述转化关系中,一定不包含_____反应(填基本类型)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,发现钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)(提出问题)黑色颗粒和白色物质是什么?
(进行猜想)甲认为黑色颗粒是炭粒,白色物质可能是Na2O或_____;乙同学还认为白色物质是氢氧化钠。甲同学立刻认为乙同学的猜想是错误的,其理由是____。
(2)(查阅资料)①Na2O为白色固体,溶于水生成氢氧化钠:Na2O + H2O = 2NaOH;②CaCl2溶液显中性。
(实验探究)甲同学对白色物质进行实验探究。
实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是____。 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(3)(反思评价)丙同学认为方案1得到的结论不正确,理由是____。
(4)(得出结论)钠在二氧化碳中燃烧的化学方程式为____。
(5)(思维托展)通过以上探究,你还能获得哪些结论,请写出一条____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com