
 С�������ȵ������Ͻ�һ��ˮ�����ִܳ�һ˿���磮��������û����������ʱ������ˮ��������Ӧ���������£�����ˮ�����ܷ�Ӧ����һ�ֳ��������������һ�����壩��С�����棬�������ʵ��̽��������ˮ������Ӧ��IJ��
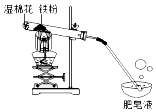
С�������ȵ������Ͻ�һ��ˮ�����ִܳ�һ˿���磮��������û����������ʱ������ˮ��������Ӧ���������£�����ˮ�����ܷ�Ӧ����һ�ֳ��������������һ�����壩��С�����棬�������ʵ��̽��������ˮ������Ӧ��IJ������ ��1�����ݷ�����Ʈ�������У�˵���ܶ�С�ڿ�������ȼ�ŵ�ľ�����������ݣ��б���������������п�ȼ�ԣ�˵�����������з�����
��2�����ݷ�Ӧ���ɺ�ɫ���壬���ܱ��������������������غ㶨�ɿ�֪����ɫ�������������������з�����
��3����������ˮ�����ڸ��µ������������������������������з�����
��� �⣺��1��������Ʈ�������У�˵���ܶ�С�ڿ�������ȼ�ŵ�ľ�����������ݣ��б���������������п�ȼ�ԣ�˵������������ѧʽΪ��H2��
��2����Ӧ���ɺ�ɫ���壬���ܱ��������������������غ㶨�ɿ�֪����ɫ��������������������ѧʽΪ��Fe3O4��
��3������ˮ�����ڸ��µ�������������������������������ѧ����ʽΪ��3Fe+4H2O$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
�ʴ�Ϊ����1��H2��
��2��Fe3O4��
��3��3Fe+4H2O$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
���� ���⿼����ǽ�������ˮ�����ķ�Ӧ��֪ʶ����ɴ��⣬�����������е�֪ʶ���У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
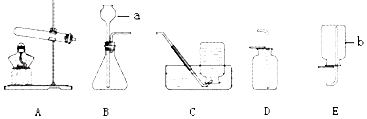
| A�� | ˮ����������������ɵ� | |
| B�� | �÷���ˮ�ɼ������ˮ��Ӳˮ������ˮ | |
| C�� | ����ˮ��ֱ������ | |
| D�� | �����ϵ�ˮ��Դ�ܷḻ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ռ�� | B�� | �������� | C�� | ���ƴ��� | D�� | ��̥��ը |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ӡ�ԭ�Ӷ��Dz��Ե��Ե����ӣ����Ե��Ե�����һ���Ƿ��ӻ�ԭ�� | |
| B�� | ������Һ��ʹ��̪��Һ��죬��ʹ��̪��Һ������Һһ���Ǽ�����Һ | |
| C�� | ȼ�ն������ŷ��⡢�������������з��⡢��������ı仯����ȼ�� | |
| D�� | �����ɽ��������Ӻ���������ӹ��ɵ����ʣ��������û�н��������ӣ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
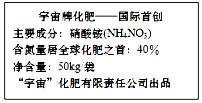 ij������������淋���ҵ������һ�����ͻ����森��ͼ��ʾ�����������Ϣ�ش��㣺
ij������������淋���ҵ������һ�����ͻ����森��ͼ��ʾ�����������Ϣ�ش��㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
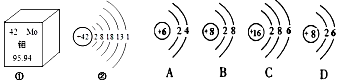
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ���� | B�� | �������� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
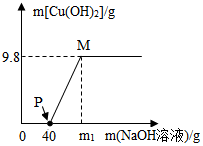 ��CuCl2��HCl��100g�����Һ�У���μ���������������Ϊ10%��NaOH��Һ���μӷ�Ӧ��NaOH��Һ���������ɳ���������ϵ��ͼ�������dz���ΪCu��OH��2�� ��ͼ�ش�
��CuCl2��HCl��100g�����Һ�У���μ���������������Ϊ10%��NaOH��Һ���μӷ�Ӧ��NaOH��Һ���������ɳ���������ϵ��ͼ�������dz���ΪCu��OH��2�� ��ͼ�ش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com