
下图是元素X的一种粒子结构示意图,下列说法正确的是
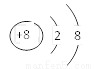
A. 该粒子是阳离子 B. X 是稀有气体元素
C. 该粒子的核电荷数是10 D. X与Mg形成的化合物为MgX
D 【解析】A、由粒子结构示意图可知,核外电子数大于核内质子数,故该粒子是阴离子,错误; B、该元素是8号元素,是氧元素,故不是稀有气体元素,错误; C、粒子的核电荷数=质子数=原子序数,故核电荷数是8,错误; D、该元素是氧元素,在化合物中显-2价,故与+2价的镁元素形成的化合物是MgO,正确。故选D。 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:山东省泰安市岱岳区2017-2018学年八年级下学期期中考试化学试卷 题型:单选题
下列有关实验现象的描述,正确的是
A. 铁丝在氧气中剧烈燃烧、火星四射、生成白色固体
B. 磷在空气中燃烧,产生大量白雾
C. 测定空气中氧气含量的实验里,铜丝加热变黑
D. 木炭在氧气中燃烧时,发出白光,生成黑色固体
C 【解析】A、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,错误;B、磷在空气中燃烧,产生大量的白烟,而不是白雾,错误;C、铜与空气中的氧气在加热条件下生成黑色的氧化铜,测定空气中氧气含量的实验里,铜丝加热变黑,正确;D、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体,错误。故选C。查看答案和解析>>
科目:初中化学 来源:四川省成都市成华区2018届九年级二诊考试化学试卷 题型:单选题
下列人体体液中,一定属于碱性的是
A. 唾液(pH 约 6.6~7.1)
B. 胃液(pH 约 0.8~1.5)
C. 胆汁(pH 约 6.8~7.4)
D. 血液(pH 约 7.35~7.45)
D 【解析】pH>7,溶液呈碱性,pH<7,溶液呈酸性,pH=7,溶液呈中性。一定属于碱性的是血液(pH 约 7.35~7.45)。故选D。查看答案和解析>>
科目:初中化学 来源:广东省广州市毕业班综合测试化学试卷 题型:填空题
锡及其化合物在生产、生活中有着重要的用途。常见的含锡物质有锡(Sn)、氧化锡(SnO2 ,也读作二氧化锡)和硫酸亚锡(SnSO4)。
(1)硫酸亚锡常用于镀锡工业。
①硫酸亚锡属于_____________(填选项)。
A.混合物 B.纯净物 C.酸 D.盐
②硫酸亚锡中锡元素的化合价是______________。
(2)SnO读作__________________。
(3)Sn+2KOH+4H2O=K2[Sn(OH)6]+2X↑,X的化学式是______________。
(4)500℃时,SnO2和氟气(F2)反应生成SnF4和O2,写出该反应的化学方程式______________。
BD +2 氧化亚锡 H2 SnO2+2F2 =SnF4+O2 【解析】(1)①硫酸亚锡是由一种物质组成的,故是纯净物,硫酸亚锡由三种元素组成的 ,且是由金属离子和酸根离子构成的,故是混合物中的盐,故选BD; ②硫酸亚锡的化学式是SnSO4,硫酸亚锡中硫酸根显-2价,根据化合价的代数和为0 ,故锡的化合价为+2价; (2)SnO中锡元素的化合价是+2价,故读作氧化亚锡; (3)根...查看答案和解析>>
科目:初中化学 来源:广东省广州市毕业班综合测试化学试卷 题型:单选题
冬天,人们常用甘油(C3H8O3)溶液护肤。下列关于甘油的说法正确的是
A. 甘油的相对分子质量为92 g B. 甘油中C、H、O三种元素的质量比是3:8:3
C. 甘油是由C3H8和O3组成的 D. 甘油中碳元素的质量分数是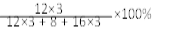
查看答案和解析>>
科目:初中化学 来源:广东省广州市毕业班综合测试化学试卷 题型:单选题
科学实验必须按规范进行操作,下列实验操作中规范的是
A.  取少量氯化钠 B.
取少量氯化钠 B.  闻药品气味 C.
闻药品气味 C. 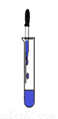 滴加液体 D.
滴加液体 D. 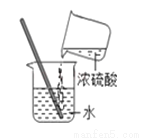 稀释浓硫酸
稀释浓硫酸
查看答案和解析>>
科目:初中化学 来源:安徽省合肥市包河区2018届九年级下学期中考模拟(一)化学试卷 题型:流程题
高铁酸钾(K2FeO4)是一种新型多功能水处理剂。下图为制取(K2FeO4)的流程,请根据图示回答下列问题:
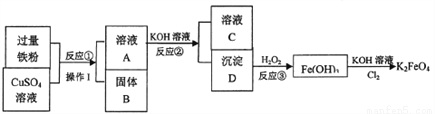
(1)固体B中含有的物质是_______________________;
(2)操作I的名称是_________,玻璃棒在操作中的作用是____________;
(3)请写出反应①的化学方程式________;反应②属于______反应(填基本反应类型);
(4)写出溶液C中溶质的一种用途_________________________。
铁和铜 过滤 引流 Fe+CuSO4=Cu+FeSO4 复分解反应 做钾肥(合理即可,如化工原料) 【解析】由题中信息知,高铁酸钾(K2FeO4)是一种新型多功能水处理剂。(1)固体B中含有的物质是铁和铜,铁比铜活泼,铁与硫酸铜溶液反应生成硫酸亚铁和铜,铁粉又过量。(2)操作I的名称是过滤,过滤是把不溶于液体的固体物质与液体分离的一种方法;玻璃棒在操作中的作用是引流,防止液体溢出。(3)反应...查看答案和解析>>
科目:初中化学 来源:广西壮族自治区钦州港经济技术开发区中学2018届春季3月份考试化学试卷 题型:实验题
暖水瓶内胆玻璃上镀有一层银,某活动小组利用废弃的暖水瓶内胆设计如图所示实验(其中分离混合物的操作已略去)。
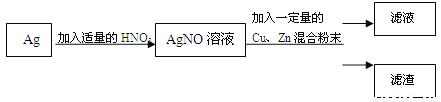
资料:Ag+2HNO 3 (浓)=AgNO 3 +NO 2 ↑+H 2 O 3Ag+4HNO 3 (稀)=3AgNO 3 +NO↑+2H 2 O
⑴根据资料,不考虑反应速率的差异,实验时选用浓硝酸还是稀硝酸?说明理由。 _________________
⑵滤渣成分可能存在多种情况,推断其中成分最简单的滤渣对应的滤液中溶质的组成。 ____________________
⑶设计实验对成分最复杂的滤渣进行验证,填写实验报告。
滤渣成分 | 实验操作及现象 |
___________ | ___________ |
查看答案和解析>>
科目:初中化学 来源:江苏省南通市如皋市2018届九年级一模化学试卷 题型:单选题
CaSO4固体受热时可分解为CaO,其化学方程式为 a CaSO4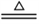 bCaO+ cSO2↑+dX↑。取2.72 g CaSO4充分加热,使之完全分解。将产生的气体通过碱石灰(CaO和NaOH的的固体混合物),碱石灰增重1.28g;再通过灼热的铜网,铜网增重0.32g。则下列说法正确的是
bCaO+ cSO2↑+dX↑。取2.72 g CaSO4充分加热,使之完全分解。将产生的气体通过碱石灰(CaO和NaOH的的固体混合物),碱石灰增重1.28g;再通过灼热的铜网,铜网增重0.32g。则下列说法正确的是
A. 剩余固体的质量为1.44g B. SO2的质量为1.6g C. X化学式可能是SO3 D. 方程式中a:c=1:1
D 【解析】A、根据质量守恒定律可知,剩余固体的质量为2.72g-1.28g-0.32g=1.12g,错误; B、碱石灰增重1.28g,增加的是二氧化硫的质量,SO2的质量为1.28g,错误; C、2.72 g CaSO4中硫元素的质量=2.72g××100%=0.64g,1.28g SO2 中硫元素的质量=1.28g××100%=0.64g,根据质量守恒定律元素的质量在化学反应...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com